Препараты класса хинолонов, используемые в клинической практике с начала 60-х годов, по механизму действия принципиально отличаются от других АМП, что обеспечивает их активность в отношении устойчивых, в том числе полирезистентных, штаммов микроорганизмов. Класс хинолонов включает две основные группы препаратов, принципиально различающихся по структуре, активности, фармакокинетике и широте показаний к применению: нефторированные хинолоны и фторхинолоны. Хинолоны классифицируют по времени введения в практику новых препаратов с улучшенными антимикробными свойствами. Согласно рабочей классификации, предложенной R. Quintiliani (1999), хинолоны разделяют на четыре поколения:
Пипемидовая (пипемидиевая) кислота
Перечисленные препараты зарегистрированы в России. За рубежом применяются и некоторые другие препараты класса хинолонов, главным образом фторхинолоны.
Хинолоны I поколения преимущественно активны в отношении грамотрицательной флоры и не создают высоких концентраций в крови и тканях.
Фторхинолоны, разрешенные для клинического применения с начала 80-х годов (II поколение), отличаются широким спектром антимикробного действия, включая стафилококки, высокой бактерицидной активностью и хорошей фармакокинетикой, что позволяет применять их для лечения инфекций различной локализации. Фторхинолоны, введенные в практику с середины 90-х годов (III-IV поколение), характеризуются более высокой активностью в отношении грамположительных бактерий (прежде всего пневмококков), внутриклеточных патогенов, анаэробов (IV поколение), а также еще более оптимизированной фармакокинетикой. Наличие у ряда препаратов лекарственных форм для в/в введения и приема внутрь в сочетании с высокой биодоступностью позволяет проводить ступенчатую терапию, которая при сопоставимой клинической эффективности существенно дешевле парентеральной.
Высокая бактерицидная активность фторхинолонов позволила разработать для ряда препаратов (ципрофлоксацин, офлоксацин, ломефлоксацин, норфлоксацин) лекарственные формы для местного применения в виде глазных и ушных капель.
Хинолоны оказывают бактерицидный эффект. Ингибируя два жизненно важных фермента микробной клетки — ДНК-гиразу и топоизомеразу IV, нарушают синтез ДНК.
Нефторированные хинолоны действуют преимущественно на грамотрицательные бактерии семейства Enterobacteriaceae
(Е.coli, Enterobacter spp., Proteus spp., Klebsiella spp., Shigella spp., Salmonella spp.), а также Haemophillus spp. и Neisseria spp. Оксолиновая и пипемидовая кислоты, кроме того, активны в отношении S.aureus и некоторых штаммов P.aeruginosa, но это не имеет клинического значения.
Фторхинолоны имеют значительно более широкий спектр. Они активны в отношении ряда грамположительных аэробных бактерий (Staphylococcus spp.), большинства штаммов грамотрицательных, в том числе Е.coli (включая энтеротоксигенные штаммы), Shigella spp., Salmonella spp., Enterobacter spp., Klebsiella spp., Proteus spp., Serratia spp., Providencia spp., Citrobacter spp., M.morganii, Vibrio spp., Haemophilus spp., Neisseria spp., Pasteurella spp., Pseudomonas spp., Legionella spp., Brucella spp., Listeria spp.
Кроме того, фторхинолоны, как правило, активны в отношении бактерий, устойчивых к хинолонам I поколения. Фторхинолоны III и, особенно, IV поколения высокоактивны в отношении пневмококков, более активны, чем препараты II поколения, в отношении внутриклеточных возбудителей (Chlamydia spp., Mycoplasma spp., M.tuberculosis, быстрорастущих атипичных микобактерий (M.avium и др.), анаэробных бактерий (моксифлоксацин). При этом не уменьшается активность в отношении грамотрицательных бактерий. Важным свойством этих препаратов является активность в отношении ряда бактерий, устойчивых к фторхинолонам II поколения. В связи с высокой активностью в отношении возбудителей бактериальных инфекций ВДП и НДП их иногда называют “респираторными” фторхинолонами.
В различной степени к фторхинолонам чувствительны энтерококки, Corynebacterium spp., Campylobacter spp., H.pylori, U.urealyticum.
Все хинолоны хорошо всасываются в ЖКТ. Пища может замедлять всасывание хинолонов, но не оказывает существенного влияния на биодоступность. Максимальные концентрации в крови достигаются в среднем через 1-3 ч после приема внутрь. Препараты проходят плацентарный барьер, и в небольших количествах проникают в грудное молоко. Выводятся из организма преимущественно почками и создают высокие концентрации в моче. Частично выводятся с желчью.
Хинолоны I поколения не создают терапевтических концентраций в крови, органах и тканях. Налидиксовая и оксолиновая кислоты подвергаются интенсивной биотрансформации и выводятся преимущественно в виде активных и неактивных метаболитов. Пипемидовая кислота мало метаболизируется и выводится в неизмененном виде. Период полувыведения налидиксовой кислоты составляет 1-2,5 ч, пипемидовой кислоты — 3-4 ч, оксолиновой кислоты — 6-7 ч. Максимальные концентрации в моче создаются в среднем через 3-4 ч.
При нарушении функции почек выведение хинолонов значительно замедляется.
Фторхинолоны, в отличие от нефторированных хинолонов, имеют большой объем распределения, создают высокие концентрации в органах и тканях, проникают внутрь клеток. Исключение составляет норфлоксацин, наиболее высокие уровни которого отмечаются в кишечнике, МВП и предстательной железе. Наибольших тканевых концентраций достигают офлоксацин, левофлоксацин, ломефлоксацин, спарфлоксацин, моксифлоксацин. Ципрофлоксацин, офлоксацин, левофлоксацин и пефлоксацин проходят через ГЭБ, достигая терапевтических концентраций.
Степень метаболизма зависит от физико-химических свойств препарата: наиболее активно биотрансформируется пефлоксацин, наименее активно — ломефлоксацин, офлоксацин, левофлоксацин. С калом выводится от 3-4% до 15-28% принятой дозы.
Период полувыведения у различных фторхинолонов колеблется от 3-4 ч (норфлоксацин) до 12-14 ч (пефлоксацин, моксифлоксацин) и даже до 18-20 ч (спарфлоксацин).
При нарушении функции почек наиболее значительно удлиняется период полувыведения офлоксацина, левофлоксацина и ломефлоксацина. При тяжелой почечной недостаточности необходима коррекция доз всех фторхинолонов. При тяжелых нарушениях функции печени может потребоваться коррекция дозы пефлоксацина.
При гемодиализе фторхинолоны удаляются в небольших количествах (офлоксацин — 10-30%, остальные препараты — менее 10%).
ЖКТ: изжога, боль в эпигастральной области, нарушение аппетита, тошнота, рвота, диарея.
ЦНС: ототоксичность, сонливость, бессонница, головная боль, головокружение, нарушения зрения, парестезии, тремор, судороги.
Аллергические реакции: сыпь, зуд, ангионевротический отек; фотосенсибилизация (наиболее характерна для ломефлоксацина и спарфлоксацина).
Гематологические реакции: тромбоцитопения, лейкопения; при дефиците глюкозо-6-фосфатдегидрогеназы — гемолитическая анемия.
Печень: холестатическая желтуха, гепатит.
Опорно-двигательный аппарат: артропатия, артралгия, миалгия, тендинит, тендовагинит, разрыв сухожилий.
Почки: кристаллурия, транзиторный нефрит.
Сердце: удлинение интервала QT на электрокардиограмме.
Другие: наиболее часто — кандидоз слизистой оболочки полости рта и/или вагинальный кандидоз, псевдомембранозный колит.
Инфекции МВП: острый цистит, противорецидивная терапия при хронических формах инфекций. Не следует применять при остром пиелонефрите.
Кишечные инфекции: шигеллез, бактериальные энтероколиты (налидиксовая кислота).
Инфекции ВДП: синусит, особенно вызванный полирезистентными штаммами, злокачественный наружный отит.
Инфекции НДП: обострение хронического бронхита, внебольничная и нозокомиальная пневмония, легионеллез.
Кишечные инфекции: шигеллез, брюшной тиф, генерализованный сальмонеллез, иерсиниоз, холера.
Менингит, вызванный грамотрицательной микрофлорой (ципрофлоксацин).
Бактериальные инфекции у пациентов с муковисцидозом.
Туберкулез (ципрофлоксацин, офлоксацин и ломефлоксацин в комбинированной терапии при лекарственноустойчивом туберкулезе).
Норфлоксацин, с учетом особенностей фармакокинетики, применяется только при кишечных инфекциях, инфекциях МВП и простатите.
Аллергическая реакция на препараты группы хинолонов.
Тяжелые нарушения функции печени и почек.
Тяжелый церебральный атеросклероз.
Аллергия. Перекрестная ко всем препаратам группы хинолонов.
Беременность. Достоверных клинических данных о токсическом действии хинолонов на плод нет. Имеются единичные сообщения о гидроцефалии, повышении внутричерепного давления и выбухании родничка у новорожденных, матери которых во время беременности принимали налидиксовую кислоту. В связи с развитием в эксперименте артропатий у неполовозрелых животных применение всех хинолонов при беременности не рекомендуется.
Кормление грудью. Хинолоны в небольших количествах проникают в грудное молоко. Есть сообщения о гемолитической анемии у новорожденных, матери которых принимали налидиксовую кислоту в период кормления грудью. В эксперименте хинолоны вызывали артропатии у неполовозрелых животных, поэтому при назначении их кормящим матерям рекомендуется перевести ребенка на искусственное вскармливание.
Педиатрия. На основании экспериментальных данных применение хинолонов не рекомендуется в период формирования костно-суставной системы. Оксолиновая кислота противопоказана детям до 2 лет, пипемидовая — до 1 года, налидиксовая — до 3 мес.
Фторхинолоны не рекомендуется назначать детям и подросткам. Однако имеющийся клинический опыт и специальные исследования применения фторхинолонов в педиатрии не подтвердили риск повреждения костно-суставной системы, в связи с чем допускается назначение фторхинолонов детям по жизненным показаниям (обострение инфекции при муковисцидозе; тяжелые инфекции различной локализации, вызванные полирезистентными штаммами бактерий; инфекции при нейтропении).
Гериатрия. У пожилых людей увеличивается риск разрыва сухожилий при применении фторхинолонов, особенно в сочетании с глюкокортикоидами.
Заболевания ЦНС. Хинолоны оказывают возбуждающее действие на ЦНС, поэтому их не рекомендуют применять пациентам с судорожным синдромом в анамнезе. Риск развития судорог повышается у больных с нарушениями мозгового кровообращения, эпилепсией и паркинсонизмом. При использовании налидиксовой кислоты возможно повышение внутричерепного давления.
Нарушения функции почек и печени. Хинолоны I поколения нельзя применять при почечной и печеночной недостаточности, так как вследствие кумуляции препаратов и их метаболитов повышается риск токсических эффектов. Дозы фторхинолонов при тяжелой почечной недостаточности подлежат коррекции.
Острая порфирия. Хинолоны не следует применять пациентам с острой порфирией, так как в эксперименте на животных они оказывают порфириногенный эффект.
При одновременном применении с антацидами и другими препаратами, содержащими ионы магния, цинка, железа, висмута, может снижаться биодоступность хинолонов вследствие образования невсасывающихся хелатных комплексов.
Пипемидовая кислота, ципрофлоксацин, норфлоксацин и пефлоксацин могут замедлять элиминацию метилксантинов (теофиллин, кофеин) и повышать риск их токсических эффектов.
Риск нейротоксических эффектов хинолонов повышается при совместном применении с НПВС, производными нитроимидазола и метилксантинами.
Хинолоны проявляют антагонизм с производными нитрофурана, поэтому следует избегать комбинаций этих препаратов.
Хинолоны I поколения, ципрофлоксацин и норфлоксацин могут нарушать метаболизм непрямых антикоагулянтов в печени, что приводит к увеличению протромбинового времени и риску кровотечений. При одновременном применении может понадобиться коррекция дозы антикоагулянта.
Следует с осторожностью назначать фторхинолоны одновременно с препаратами, удлиняющими интервал QT, так как увеличивается риск развития сердечных аритмий.
При одновременном применении с глюкокортикоидами повышается риск разрыва сухожилий, особенно у пожилых людей.
При использовании ципрофлоксацина, норфлоксацина и пефлоксацина совместно с препаратами, ощелачивающими мочу (ингибиторы карбоангидразы, цитраты, натрия бикарбонат), увеличивается риск кристаллурии и нефротоксических эффектов.
При одновременном применении с азлоциллином и циметидином в связи с понижением канальцевой секреции замедляется элиминация фторхинолонов и повышаются их концентрации в крови.
Препараты хинолонов при приеме внутрь следует запивать полным стаканом воды. Принимать не менее чем за 2 ч до или через 6 ч после приема антацидов и препаратов железа, цинка, висмута.
Строго соблюдать режим и схемы лечения в течение всего курса терапии, не пропускать дозу и принимать ее через равные промежутки времени. В случае пропуска дозы принять ее как можно скорее; не принимать, если почти наступило время приема следующей дозы; не удваивать дозу. Выдерживать длительность терапии.
Не использовать препараты с истекшим сроком годности.
В период лечения соблюдать достаточный водный режим (1,2-1,5 л/сут).
Не подвергаться прямому воздействию солнечных и ультрафиолетовых лучей во время применения препаратов и в течение не менее 3 дней после окончания лечения.
Проконсультироваться с врачом, если улучшение не наступает в течение нескольких дней или появляются новые симптомы. При появлении боли в сухожилиях следует обеспечить покой пораженному суставу и обратиться к врачу.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Введение Появление хинолоновых антибиотиков ведет свое начало с открытия в 1962 г. в процессе синтеза хлорохина налидиксовой кислоты (рис. 1). На протяжении двух десятилетий налидиксовая кислота и ее производные (пипемидиевая и оксолиниевая кислоты), обладающие активностью в отношении грамотрицательных микроорганизмов, с успехом использовались для лечения инфекций мочевыводящих путей. Вторая волна развития хинолонов (1980–е гг.) связана с появлением фторированных соединений с более высокой активностью в отношении грамотрицательных, некоторых грамположительных бактерий и внутриклеточных микроорганизмов, обладающих улучшенной фармакокинетикой, наличием форм для парентерального введения (ципрофлоксацин, офлоксацин, флероксацин, ломефлоксацин, норфлоксацин) [1]. Однако низкая антипневмококковая активность препаратов II поколения хинолонов в настоящее время делает невозможным их применение при большинстве инфекций дыхательных путей. Следующий этап развития хинолонов (1990–е гг.) связан с появлением ди– и трехфторированных соединений, обладающих усиленной активностью в отношении грамположительных бактерий (особенно Streptococcus pneumoniae) и внутриклеточных возбудителей. Данное качество обусловило название этих препаратов – «респираторные» фторхинолоны, – относимых согласно современной классификации к III (спарфлоксацин, левофлоксацин) и IV (моксифлоксацин, гатифлоксацина, гареноксацин) поколениям хинолонов. В Российской Федерации зарегистрированы три препарата – левофлоксацин, моксифлоксацин и гемифлоксацин.
Появление хинолоновых антибиотиков ведет свое начало с открытия в 1962 г. в процессе синтеза хлорохина налидиксовой кислоты (рис. 1). На протяжении двух десятилетий налидиксовая кислота и ее производные (пипемидиевая и оксолиниевая кислоты), обладающие активностью в отношении грамотрицательных микроорганизмов, с успехом использовались для лечения инфекций мочевыводящих путей. Вторая волна развития хинолонов (1980–е гг.) связана с появлением фторированных соединений с более высокой активностью в отношении грамотрицательных, некоторых грамположительных бактерий и внутриклеточных микроорганизмов, обладающих улучшенной фармакокинетикой, наличием форм для парентерального введения (ципрофлоксацин, офлоксацин, флероксацин, ломефлоксацин, норфлоксацин) [1]. Однако низкая антипневмококковая активность препаратов II поколения хинолонов в настоящее время делает невозможным их применение при большинстве инфекций дыхательных путей. Следующий этап развития хинолонов (1990–е гг.) связан с появлением ди– и трехфторированных соединений, обладающих усиленной активностью в отношении грамположительных бактерий (особенно Streptococcus pneumoniae) и внутриклеточных возбудителей. Данное качество обусловило название этих препаратов – «респираторные» фторхинолоны, – относимых согласно современной классификации к III (спарфлоксацин, левофлоксацин) и IV (моксифлоксацин, гатифлоксацина, гареноксацин) поколениям хинолонов. В Российской Федерации зарегистрированы три препарата – левофлоксацин, моксифлоксацин и гемифлоксацин.
«Респираторные» фторхинолоны высокоэффективны в отношении всех потенциальных возбудителей внебольничной пневмонии (ВП) (табл. 1), оказывают бактерицидное действие и обладают выраженным постантибиотическим эффектом, который в среднем равен 2 ч.
Все «респираторные» фторхинолоны имеют длительный период полувыведения, что позволяет принимать их 1 раз/сут., характеризуются высокой биодоступностью и быстрой абсорбцией. Антимикробное действие фторхинолонов зависит от создаваемых концентраций антибиотика, при этом наилучшим фармакодинамическим параметром, коррелирующим с эрадикацией бактерий, является отношении AUC (не связанной с белками фракции антибиотика) к МПК. Надежным предиктором эрадикации S. pneumoniae является отношение свободной AUC/МПК ≥ 25. У левофлоксацина, моксифлоксацина и гемифлоксацина этот показатель составляет 40, 96 и 97–127 соответственно (табл. 2) [5,6].
«Респираторные» фторхинолоны обладают высокой тканевой пенетрацией, создавая в альвеолярных макрофагах, слизистой бронхов и жидкости, выстилающей эпителий дыхательных путей, концентрации, существенно превосходящие МПК чувствительных к ним возбудителей респираторных инфекций.
Резистентность актуальных для инфекций дыхательных путей микроорганизмов к «респираторным» фторхинолонам во всем мире, за исключением ряда стран Юго–Восточной Азии, остается невысокой [7]. Так, в Европе более 97% штаммов S. pneumoniae чувствительны к «респираторным» фторхинолонам [8], а в России до настоящего времени было выделено лишь по одному штамму с умеренной резистентностью к левофлоксацину и моксифлоксацину [9]. До настоящего времени в РФ не было выделено ни одного штамма H. influenzae, резистентного к «респираторным» фторхинолонам.
История создания и последующего клинического применения фторхинолонов является показательной иллюстрацией того, что по мере расширения спектра и усиления антимикробного действия возрастает и частота серьезных нежелательных явлений, что послужило причиной изъятия отдельных препаратов с фармацевтического рынка (грепафлоксацин, тровафлоксацин, клинафлоксацин и др.) [10]. В отношении левофлоксацина (Таваник) известно, что за период использования более чем у 300 млн пациентов во всем мире не было зафиксировано серьезных проблем с безопасностью. Напротив, для гемифлоксацина данная проблема является основной, так как в процессе его применения зарегистрировано появление кожной сыпи (макулопапулезной) при длительных курсах его приема женщинами моложе 40 лет и женщинами в постменопаузальном периоде, находящимися на заместительной гормональной терапии. В этой связи не рекомендуется назначать препарат курсами более 7 дней. Гемифлоксацин может приводить к удлинению интервала QT, в связи с чем не рекомендуется для использования у пациентов с удлинением интервала QT в анамнезе, электролитным дисбалансом и принимающих антиаритмические препараты IА и III классов [11]. Кроме того, пока еще малый срок клинического применения препарата не позволяет в полной мере оценить безопасность его применения.
У левофлоксацина (Таваник) и моксифлоксацина есть лекарственные формы, как для перорального, так и для парентерального применения, что позволяет их использовать в режиме ступенчатой терапии, например у пациентов со среднетяжелым и тяжелым течением пневмонии. Гемифлоксацин доступен только лишь для перорального приема, что ограничивает его применение нетяжелыми формами заболевания.
Клиническое применение
«респираторных» фторхинолонов
Внебольничная пневмония
В этиологии ВП преимущественное значение имеет Streptococcus pneumoniae, на долю которого приходится 30–50% случаев заболевания. «Атипичные» микроорганизмы – Chlamydophila pneumoniae, Mycoplasma pneumoniae, Legionella pneumophila – ответственны за развитие 8–30% случаев ВП. К типичным возбудителям относятся Haemophilus influenzae, Staphylococcus aureus, Klebsiella pneumoniae, ответственные за 3–5% случаев ВП, реже встречаются случаи заболевания, ассоциируемые с другими энтеробактериями и неферментирующими грамотрицательными микроорганизмами. Этиологическая структура ВП может различаться в зависимости от возраста больных, тяжести заболевания, наличия сопутствующей патологии. У пациентов, госпитализированных в терапевтическое отделение, в этиологии ВП преобладают пневмококки, на долю Chlamydophila и Mycoplasma pneumoniae суммарно приходится порядка 25%. Напротив, последние не имеют существенного значения в этиологии тяжелой ВП, требующей лечения в отделении реанимации и интенсивной терапии (ОРИТ); в то же время у этой категории больных возрастает роль Legionella spp., а также S. aureus и грамотрицательных энтеробактерий [12].
Антибактериальная терапия ВП должна проводиться сразу после установления диагноза заболевания, задержка с началом антибиотикотерапии ведет к ухудшению прогноза заболевания. В подавляющем большинстве случаев антибиотик назначается эмпирически, что требует знания спектра наиболее вероятных возбудителей и локальной эпидемиологии резистентности.
При выборе конкретного антибиотика необходимо учитывать следующие факторы: антимикробную активность в отношении потенциальных возбудителей ВП; высокую биодоступность с учетом возрастных особенностей пациента; приемлемый профиль безопасности; оптимальный режим дозирования (кратность приема не превышает 2 раз/сут., в противном случае возрастает риск невыполнения режима лечения); минимальный уровень лекарственных взаимодействий.
Рекомендации по эмпирической антибактериальной терапии ВП представлены на рисунке 2. Среди пациентов с нетяжелой ВП (лечение в амбулаторных условиях) выделяют 2 группы, которые различаются между собой по этиологической структуре и тактике антибактериальной терапии. В первую группу включены пациенты без сопутствующих заболеваний, не принимавшие в последние 3 мес. антибактериальные препараты, т.е. пациенты без так называемых факторов риска терапевтической неудачи. В качестве средств выбора в данной ситуации рекомендуются амоксициллин или «современные» макролидные антибиотики. Макролидам следует отдавать предпочтение при непереносимости β –лактамных антибиотиков или при подозрении на атипичную этиологию заболевания (M. pneumoniae, C. pneumoniae).
Во вторую группу включены пациенты, получавшие в последние 3 мес. антибактериальные препараты и больные сопутствующими заболеваниями (ХОБЛ, сахарный диабет, застойная сердечная недостаточность, заболевания печени, злоупотребление алкоголем, наркомания, дефицит массы тела, курение). Учитывая вероятность участия в этиологии заболевания грамотрицательных микроорганизмов (в том числе обладающих некоторыми механизмами антибиотикорезистентности), а также ко–инфекции, пациентам данной группы рекомендовано проведение комбинированной терапии – «защищенный» аминопенициллин + макролид. Также возможно применение «респираторных» фторхинолонов (Таваник, моксифлоксацин, гемифлоксацин).
У пациентов, госпитализированных в отделение общего профиля, рекомендуется проведение комбинированной терапии β –лактам + макролид, так как наличие в стартовом режиме терапии препарата, активного в отношении «атипичных» микроорганизмов, улучшает прогноз и сокращает продолжительность пребывания пациентов в стационаре. В случае неэффективности проводимой терапии, при наличии факторов риска антибиотикорезистентных микроорганизмов (пожилой возраст, сопутствующая патология, иммуносупрессия и пр.), пациенты с факторами риска грамотрицательных энтеробактерий, проводимое ранее лечение β –лактамными антибиотиками, пневмония у пациентов, проживающих в домах престарелых, целесообразно использование «респираторных» фторхинолонов в режиме ступенчатой терапии [13].
Больным с тяжелым течением заболевания рекомендуется проведение комбинированной терапии β –лактам в/в + макролид в/в, либо парентеральные формы «респираторных» фторхинолонов в комбинации с цефалоспоринами III–IV поколения (цефотаксим, цефтриаксон, цефепим).
Наибольшие трудности при лечении ВП возникают в случае присутствия антибиотикорезистентных штаммов пневмококка, при тяжелом течении пневмонии (^ роль S. aureus и семейства Enterobacteriaceae), а также у больных пожилого и старческого возраста. Именно в вышеуказанных ситуациях наиболее часто отмечаются неэффективность антибактериальной терапии, развитие осложнений заболевания, высокая летальность. Факторы риска лекарственноустойчивых/проблемных возбудителей внебольничной пневмонии представлены на рисунке 3. Стоит отметить, что, согласно имеющимся современным данным, клинически значимый уровень резистентности S. pneumoniae к пенициллину наблюдается у штаммов с МПК не менее 4 мг/л [14]. Важно, что, согласно результатам отдельных исследований, резистентность к макролидам и фторхинолонам (ципрофлоксацин) может быть причиной терапевтической неудачи, в то же время случаев неэффективности терапии ВП «новыми» фторхинолонами (левофлоксацин, моксифлоксацин, гемифлоксацин), обусловленной антибиотикорезистентностью, не зарегистрировано.
В этой связи указанные ситуации требуют преимущественного назначения «респираторных» фторхинолонов. При наличии факторов риска P. aeruginosa препаратом выбора является левофлоксацин (Таваник).
Перспективы применения «респираторных» фторхинолонов связаны с рядом исследований, в которых было показано, что применение данных препаратов сопровождается меньшей, по сравнению с другими режимами антибиотикотерапии, неэффективностью лечения (табл. 3) [18,19]. Очевидно, что применение «респираторных» фторхинолонов обусловливает лучший исход заболевания за счет своей высокой активности в отношении всех потенциальных возбудителей ВП, включая «атипичные» микроорганизмы (C. pneumoniae, M. pneumoniae и L. pneumophila), а также вследствие выраженной антипневмококковой активности, включая лекарственноустойчивые штаммы данного микроорганизма [16]. В этом отношении интересными являются данные исследования, показавшего, что применение левофлоксацина у пациентов с тяжелой пневмококковой пневмонией сопровождается более коротким временем достижения клинической стабильности, чем антибактериальная терапия цефтриаксоном [17].
Обострение ХОБЛ
Хроническая обструктивная болезнь легких (ХОБЛ) является одной из наиболее актуальных проблем современного здравоохранения, ввиду широкой распространенности с отчетливой тенденцией к увеличению числа больных и смертности. Важнейшим фактором, определяющим темпы прогрессирования бронхиальной обструкции, а также качество жизни больных и величину экономических затрат является частота обострений [20,21]. Пациенты с ХОБЛ переносят от 1 до 4 и более обострений в течение года, при этом в более чем половине случаев требуется лечение в условиях стационара.
В подавляющем числе случаев (75–80%) обострение ХОБЛ имеет инфекционную природу. Основными возбудителями являются H. influenzae, S. pneumoniae и Moraxella catarrhalis (табл. 1) [22,23]. Реже из образцов мокроты больных ХОБЛ выделяют Haemophilus parainfluenzae, S. aureus, P. aeruginosa и представителей семейства Enterobacteriaceae [24,25]. Удельный вес «атипичных» возбудителей – M. pneumoniae и C. pneumoniae – в развитии обострений составляет порядка 5%. Порядка 30% обострений ХОБЛ имеют вирусную природу [26]. Чаще всего выявляют риновирусы – 20–25%, реже вирусы гриппа – 3–10%. Кроме всего прочего, доказано, что вирусная инфекция служит «проводником» развития обострения в более чем 50% случаев [27].
Тяжесть обострения ХОБЛ корреспондирует с типом инфекционного агента. У пациентов с легким обострением ХОБЛ обострение чаще всего обусловлено S. pneumoniae, по мере прогрессирования болезни (снижение объема форсированного выдоха за 1 с – ОФВ1, частые обострения в течение года, курильщики) выявляют H. influenzae, M. catarrhalis и Enterobacteriaceae [28,30]. В случае тяжелого обострения нередко обнаруживают P. aeruginosa. Факторами риска синегнойной инфекции являются выраженная бронхиальная обструкция (ОФВ1 ≥ 2 дней в течение прошлых 90 дней); частое применение антибиотиков ( ≥ 4 курсов в течение года).
Эмпирическая антибиотикотерапия инфекционного обострения ХОБЛ предусматривает выбор препаратов, активных в отношении наиболее вероятных бактериальных возбудителей с учетом распространенности механизмов приобретенной устойчивости к различным классам антибиотиков. С учетом вышеперечисленных требований в лечении инфекционного обострения ХОБЛ применяются β –лактамные антибиотики, макролиды и «респираторные» фторхинолоны. Эволюция отношения к вышеперечисленным классам антибиотиков берет свое начало с мета–анализа, выполненного Siempos I. и соавт., 2007 [29], в ходе которого проводилась сравнительная оценка эффективности и безопасности использования макролидов, «респираторных» фторхинолонов и амоксициллина/клавуланата в терапии обострения ХОБЛ. В результате мета–анализа все перечисленные антибиотики продемонстрировали сравнимую клиническую эффективность, при этом было отмечено, что использование «респираторных» фторхинолонов характеризовалось более высокой микробиологической эффективностью и меньшей частотой рецидивов заболевания по сравнению с макролидами, тогда как прием амоксициллина/клавуланата сопровождался наиболее высокой частотой развития нежелательных явлений по сравнению с другими препаратами.
Очевидно, что в настоящий момент времени наиболее важным критерием эффективности антибиотикотерапии при ХОБЛ является длительность периода между обострениями. С этой точки зрения, наибольшие перспективы связаны с применением именно «респираторных» фторхинолонов, что доказано в целом ряде клинических исследований [32–35]. Наличие у данной группы антибиотиков высокой бактерицидной активности по отношению к грамположительным и грамотрицательным микроорганизмам, включая лекарственноустойчивые штаммы S. pneumoniae, обеспечивает максимальную степень эрадикации возбудителей обострения ХОБЛ. Важной особенностью «респираторных» фторхинолонов является способность оказывать бактерицидное действие на покоящиеся формы бактерий, формирующих биопленки. Подобный эффект продемонстрирован в отношении H. influenzae и P. aeruginosa (для левофлоксацина) [31,36,37].
Отечественными экспертами [38] в настоящее время предлагается подход к ведению пациентов с инфекционным обострением ХОБЛ, представленный на рисунке 4. Антибиотиками выбора у пациентов с простым/неосложненным обострением ХОБЛ1 являются амоксициллин, «современные» макролиды (азитромицин, кларитромицин) и цефуроксима аксетил. Напротив, в группе пациентов, переносящих осложненное обострение ХОБЛ2, рекомендуется применение «респираторных» фторхинолонов (Таваник, моксифлоксацин, гемифлоксацин) или ингибиторозащищенных пенициллинов. Присутствие же факторов риска синегнойной инфекции (ОФВ1 ≤ 5 дней) при нетяжелой ВП, неосложненном обострении ХОБЛ также приводит к улучшению комплаентности пациентов [42].
источник
Респираторные фторхинолоны – расширение терапевтических возможностей в лечении респираторных инфекций
Респираторные инфекции нижних отделов дыхательных путей — пневмония и обострения хронического бронхита — являются одной из самых частых причин обращения за врачебной помощью и назначения антибиотиков. Выбирая антимикробный препарат, врач исходит из ряда
Респираторные инфекции нижних отделов дыхательных путей — пневмония и обострения хронического бронхита — являются одной из самых частых причин обращения за врачебной помощью и назначения антибиотиков. Выбирая антимикробный препарат, врач исходит из ряда критериев. К наиболее важным из них относятся эффективность и безопасность. Эффективность определяется активностью антибиотика в отношении наиболее распространенных возбудителей инфекций нижних отделов респираторного тракта. Среди возбудителей пневмонии наиболее часто встречаются пневмококки, гемофильная палочка, атипичные возбудители — хламидии и микоплазма, а при тяжелом течении — легионелла. У пожилых и стариков, больных сахарным диабетом, хронической обструктивной болезнью легких (ХОБЛ), с нарушенной функцией почек, злоупотребляющих алкоголем возрастает частота таких возбудителей, как клебсиеллы и стафилококки.
Этиология внебольничных пневмоний:
- Streptococcus (Str.) pneumoniae — 20-60%;
- Mycoplasma pneumoniae — 5-50%;
- Сhlamidia pneumoniae — 5-15%;
- Haemophilus (H.) influenzae — 3-10%;
- Бактерии семейства Enterobacteriaceae:
Klebsiella (K.) pneumoniae, Escherichia (E.) coli — 3-10%; - Staphylococcus (S.) aureus — 3-10%;
- Другие (S. pyogenes, Legionella pneumoniae).
Среди этиологических факторов при инфекционных обострениях ХОБЛ доминируют пневмококки и грамотрицательные возбудители: гемофильная палочка, моракселла катаралис. Больные ХОБЛ после стационарного лечения могут быть инфицированы госпитальной микрофлорой (клебсиелла, стафилококки, синегнойная палочка), резистентной к широко применяемым антибактериальным препаратам.
Перечислим наиболее вероятных возбудителей для определенных групп больных:
- старше 65 лет, без сопутствующих заболеваний: H. influenzae, Str. рneumoniae, Moraxella catarrhalis;
- от 65 лет и старше и/или с сопутствующими заболеваниями или обострениями > 2 раз в год: H. influenzae, Str. pneumoniae, K. pneumoniae, E. сoli;
- пациенты с бронхоэктазами, тяжелым течением ХОБЛ: K. рneumoniae, E. сoli, S. aureus, H. influenzae, Pseudomonas (P.) aeruginosa.
В последние годы наблюдается рост резистентности возбудителей респираторных инфекций. Внушает тревогу прежде всего устойчивость пневмококков к пенициллину, при этом штаммы, устойчивые к пенициллину, приобретают устойчивость и к макролидам, ко-тримоксазолу, тетрациклину, фторхинолонам (табл. 1).
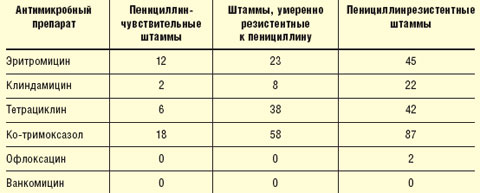 |
| Таблица 1 Перекрестная устойчивость пенициллинустойчивых пневмококков к другим антибактериальным препаратам, % (B. Murray, 1997) |
При этом от 20 до 40% штаммов гемофильной палочки продуцируют β-лактамазы, что делает их устойчивыми к действию аминопенициллинов. Следует отметить, что распространенность антибиотикорезистентности в разных странах и в разных регионах различаются. В России, по данным исследования «Пегас-1», умеренно резистентные и резистентные к пенициллину штаммы пневмококков составили 11% (Л. С. Страчунский, 2001). По данным того же исследования, резистентность гемофильной палочки к аминопенициллинам в России не представляет значительной проблемы. В то же время исследования, проведенные В. С. Сидоренко и соавт. (2001), показали, что в Москве резистентность пневмококков значительно выше — до 24%. Это еще раз подтверждает важность проведения локального мониторинга чувствительности возбудителей респираторных инфекций и формирования регионарных формулярных списков.
β-лактамные антибиотики (пенициллины, цефалоспорины) малоактивны в отношении штаммов пневмококков, резистентных к пенициллину, и не действуют на атипичных возбудителей. Значение макролидов при лечении респираторных инфекций снижается как ввиду роста резистентности пневмококков, так и недостаточной активности этих антибиотиков в отношении гемофильной палочки и отсутствия действия на микроорганизмы грамотрицательных возбудителей семейства Enterobacteriaceae. Классические фторхинолоны обладают относительно невысокой активностью в отношении пневмококков. Таким образом, рост резистентности возбудителей, увеличение ассоциаций возбудителей, особенно у больных с тяжелым течением заболевания и сопутствующей патологией (Л. А. Алексанян, 1999; А. А. Чибикова, 2005), потребовали расширения перечня препаратов для терапии респираторных инфекций.
«Новые» фторхинолоны относятся именно к таким препаратам. В чем же их отличие от «старых» фторхинолонов?
В настоящее время фторхинолоны делятся на четыре группы (классификация German Paul Ehrlich, 1998).
- Фторхинолоны, активные в отношении грамотрицательных возбудителей, с ограниченными показаниями к применению, в основном при мочевых инфекциях.
- «Классические» фторхинолоны, с широкими показаниями к применению, активные в отношении грамотрицательных, атипичных возбудителей, метициллинчувствительных стафилококков, но обладающие слабой активностью в отношении пневмококков (ципрофлоксацин, офлоксацин).
- «Новые» фторхинолоны с повышенной активностью в отношении пневмококков и атипичных возбудителей и с сохраненной активностью в отношении грамотрицательных возбудителей (левофлоксацин, спарфлоксацин).
- «Новые» фторхинолоны с повышенной активностью в отношении пневмококков и атипичных возбудителей, активностью в отношении грамотрицательных микроорганизмов и умеренной активностью в отношении анаэробных возбудителей (моксифлоксацин, гатифлоксацин).
Фторхинолоны III и IV поколений, сохраняя активность в отношении грамотрицательных возбудителей, более активны в отношении грамположительных кокков и атипичных возбудителей. In vitro они проявляют активность против метициллинрезистентных стафилококков. В связи с высокой активностью в отношении возбудителей респираторной инфекции они получили название «респираторные» фторхинолоны. В отношении P. aeruginosa они менее активны, чем ципрофлоксацин. Возбудители, устойчивые к фторхинолонам II поколения, могут быть чувствительны к фторхинолонам III–IV поколений. Фторхинолоны IV поколения умеренно активны в отношении анаэробов.
Фторхинолоны обладают быстрым бактерицидным эффектом, нарушая синтез дезоксирибонуклеиновой кислоты (ДНК) микробной клеткой путем ингибирования ферментов ДНК-гиразы и топоизомеразы IV, при этом образование ДНК в клетках организма человека не подавляется. Ингибирование функции топоизомераз приводит к необратимым изменениям в микробной клетке и ее гибели.
Фторхинолоны обладают умеренно выраженным постантибиотическим действием, под которым понимают стойкое подавление роста бактерий после ограниченного воздействия на него антимикробного препарата, при этом длительность постантибиотического эффекта зависит от вида микроорганизма и дозы [5]. Резистентность микроорганизмов к фторхинолонам развивается медленно по типу хромосомной и связана с мутациями по генам, кодирующим ДНК-гиразу или топоизомеразу IV. Уровень резистентности бывает более высоким при многоступенчатых мутациях. При этом резистентность развивается только к хинолонам. Новые фторхинолоны гораздо меньше способствуют селекции резистентных штаммов, так как чем больше активность фторхинолона по отношению к обоим ферментам, тем ниже уровень резистентности, который зависит от мутации в генах, кодирующих один фермент [6].
Эффективность антибиотика зависит также и от его фармакокинетических параметров. Всем фторхинолонам свойственны высокая биодоступность при приеме внутрь, большой объем распределения, низкое связывание с сывороточными белками, хорошее проникновение в органы, ткани и клетки организма человека, длительная циркуляция в организме, элиминация почечными и внепочечными механизмами. Биодоступность новых фторхинолонов близка к 100%; пища замедляет, но не снижает их всасываемость. Максимальная концентрация в крови достигается через 1–3 ч после приема. Они имеют большой объем распределения, создают высокие концентрации в тканях и жидкостях организма, проникают внутрь клеток, в полиморфноядерные нейтрофилы, макрофаги, альвеолярные макрофаги, где их концентрации в 2–12 раз превышают внеклеточные концентрации [7]. Респираторные фторхинолоны достигают высоких концентраций в бронхиальном секрете, что является предпосылкой для эрадикации внеклеточно расположенных возбудителей, а высокие внутриклеточные концентрации важны при пневмонии, вызванной атипичными возбудителями; они связываются с белками плазмы на 20–40%. Фторхинолоны проходят через плаценту, проникают в грудное молоко.
Препараты мало подвержены печеночному метаболизму, период полувыведения колеблется от 3–6 ч (левофлоксацин) до 10–12 ч (моксифлоксацин), что позволяет назначать их 1–2 раза в сутки. Выводятся через почки и кишечник, при этом почечная элиминация преобладает у левофлоксацина, и при нарушении функции почек период полувыведения значительно удлиняется. При тяжелой почечной недостаточности требуется коррекция доз всех фторхинолонов. При гемодиализе фторхинолоны удаляются в малой степени. С возрастом фармакокинетические параметры фторхинолонов меняются мало, поэтому коррекции доз у пациентов старших возрастных групп не требуется. В то же время у этих пациентов может быть снижена функция почек, что может привести к повышению концентрации антибиотика в крови [8].
Для фторхинолонов предиктором эффективности является отношение площади под фармакокинетической кривой к минимальной подавляющей концентрации (МПК). При лечении пневмококковой инфекции этот коэффициент должен быть более 30, а при грамотрицательных возбудителях — более 100 [9]. Этот коэффициент 30–44 — для левофлоксацина, значительно выше — для моксифлоксацина и чуть более 10 — при приеме максимальной суточной дозы ципрофлоксацина (табл. 2). Эти данные еще раз подтверждают, что ципрофлоксацин малоэффективен при инфекциях, вызванных пневмококками, и не может быть препаратом первого ряда при респираторных амбулаторных инфекциях.
 |
| Таблица 2 Отношение площади под кривой «концентрация — время (AUC)» к минимальной подавляющей концентрации для фторхинолонов (AUC/МПК90 для фторхинолонов в отношении пневмококков) |
Безопасность антибиотикотерапии определяется частотой и тяжестью развития нежелательных действий препарата и риском развития нежелательных лекарственных и диетических взаимодействий. При применении респираторных фторхинолонов нежелательные эффекты развиваются нечасто. В большинстве случаев это проявления диспепсии (тошнота, рвота, диарея); могут отмечаться головная боль, головокружения, нарушения сна. У пожилых и старых людей, особенно на фоне приема системных глюкокортикостероидов, существует риск разрыва сухожилий. Может отмечаться преходящее повышение активности печеночных ферментов. В единичных случаях описано развитие анафилактического шока, судорожного синдрома. Риск развития артропатий ограничивает их применение у беременных и кормящих, а также у детей.
Антацидные препараты, содержащие алюминий и магний, снижают всасывание фторхинолонов из желудочно-кишечного тракта, поэтому перерыв во времени между приемом антацида и антибиотика должен составлять не менее 2 ч. Не отмечено взаимодействия с ферментной системой цитохрома Р450 [9].
Эффективность антибиотикотерапии во многом зависит от соблюдения пациентом режима терапии, от того, насколько он следует рекомендациям врача. Сложность режима приема препарата (связь с приемом пищи, частота приема, количество препаратов), нежелательные действия (в том числе легкие, которые, по мнению врача, не требуют отмены препарата) могут спровоцировать больного на прекращение лечения. Как показали результаты фармакоэпидемиологического исследования, примерно 50% взрослых прекращали антибактериальную терапию преждевременно, а более 10% не следовали рекомендуемому режиму дозирования. Среди родителей 18,7% заканчивали антибактериальную терапию у детей преждевременно (не придерживались рекомендуемого врачом курса). Таким образом, результаты проведенного исследования показали, что взрослое население характеризируется неудовлетворительной комплаентностью в отношении рекомендуемой длительности курса антибактериальной терапии [10]. При проведении исследования по оценке сравнительной эффективности коротких (5-дневных) курсов левофлоксацина и 7-дневных было показано, что эффективность первых курсов не отличается от последних: при обоих режимах лечения отмечалась равная клиническая и микробиологическая эффективность [11]. С этих позиций респираторные фторхинолоны, которые можно принимать однократно в сутки, независимо от приема пищи и короткими курсами, имеют преимущества перед многими другими антибактериальными препаратами и их назначение повышает комплаентность пациентов.
Наличие форм для парентерального и перорального введения повышают удобство использования препаратов и делают возможным их использование в режиме ступенчатой терапии.
Клиническая, бактериологическая эффективность и безопасность респираторных фторхинолонов была оценена во многих многоцентровых клинических исследованиях. Так, по данным метаанализа пяти клинических исследований, прием моксифлоксацина в дозе 400 мг 1 раз в сутки при респираторных инфекциях по клинической эффективности не отличался от амоксициллина в дозе 1000 мг 3 раза в сутки и кларитромицина в дозе 500 мг 2 раза в сутки. Бактериологическая эффективность моксифлоксацина была выше и составила 94%. При использовании левофлоксацина при лечении пациентов с пневмонией препарат применяли в суточной дозе 500 мг. В исследование включили 68 больных; у 26 была пневмония тяжелого течения — у них левофлоксацин применяли в режиме ступенчатой терапии. Клиническая и бактериологическая эффективность препарата составила 100%. Только в одном случае (1,4%) потребовалась его отмена из-за преходящих нарушений психики [12]. В исследовании C. Fogarty et al. (1999) эффективность и безопасность терапии моксифлоксацином в дозе 400 мг в сутки в течение 10 дней сравнивали с эффективностью и безопасностью кларитромицина в дозе 500 мг в сутки в течение 10 дней. В исследование были включены 382 пациента с внебольничной пневмонией. Оба препарата оказались сопоставимы как по эффективности, так и по частоте развития нежелательных действий. Эффективность лечения составила 95%. В исследование по сравнению эффективности моксифлоксацина и кларитромицина у больных ХОБЛ были включены 750 пациентов (R. Wilson et al., 1999). Пациенты получали моксифлоксацин в дозе 400 мг/сут в течение 5 дней или кларитромицин в дозе 500 мг 2 раза в сутки в течение 7 дней. Клиническое выздоровление отмечалось у 89% пациентов, получавших моксифлоксацин, и у 88% пациентов, принимавших кларитромицин. Через месяц после окончания курса терапии клиническая эффективность подтверждена у 89% пациентов обеих групп. При этом бактериологическая эффективность моксифлоксацина была достоверно выше: 77,4 и 62,3% соответственно. Российские авторы сравнивали эффективность лечения обострения хронического бронхита левофлоксацином в дозе 500 мг/сут в течение 7 дней и цефуроксим аксетилом в дозе 250 мг 2 раза в сутки в течение 10 дней. Клиническая эффективность препаратов не отличалась и составила 92% в обеих группах, тогда как бактериологическая эффективность была выше в группе принимавших левофлоксацин и составила 94% против 87% в группе лечения цефуроксим аксетилом [14].
В заключение следует отметить, что респираторные фторхинолоны высокоактивны в отношении наиболее распространенных возбудителей пневмонии и обострения хронического бронхита, в том числе штаммов, устойчивых к β-лактамам, макролидам. Препараты обладают высокой биодоступностью при приеме внутрь, быстро всасываются, создают высокие концентрации в легочной ткани, бронхолегочном секрете, в клетках организма человека. Они обладают длительным периодом полувыведения, что позволяет принимать их 1–2 раза в сутки, выпускаются в виде форм для парентерального и перорального приема, что дает возможность использовать их в режиме ступенчатой терапии. Эффективность коротких 5-дневных курсов сопоставима с эффективностью более длительных курсов антибактериальной терапии. Препараты хорошо переносятся, обладают минимальным количеством нежелательных лекарственных и диетических взаимодействий.
По вопросам литературы обращайтесь в редакцию.
Е. А. Прохорович, доктор медицинских наук, профессор
МГМСУ, Москва
источник
Фторхинолоны – препараты относятся к группе хинолонов и обладают антибактериальными свойствами. Используются в клинической практике пульмонологии, отоларингологии, урологии, нефрологии, дерматологии, офтальмологии. Широта применения обусловлена спектром действия, эффективностью этих лекарственных средств. При этом они обладают рядом негативных влияний. Своевременное назначение антибиотиков строго по показаниям, в должных дозировках, с учетом противопоказаний обеспечивает эффективность, а также безопасность терапии.

Список препаратов различных фторхинолонов и хинолонов насчитывает около 4 десятков средств. Они разделяются по наличию или отсутствию атома фтора, по количеству его в молекуле (монофтохинолоны, дифтохинолоны), по преимущественному спектру действия (грамотрицательные, анаэробные), области применения (респираторные).
Наиболее полная картина содержится при классификации хинолонов на отдельные поколения. Именно такой подход распространен на практике.
Общая классификация хинолонов:
- 1 поколение (нефторированные): налидиксовая кислота, оксолиновая кислота;
- 2 поколение (грамотрицательные): ципрофлоксацин, норфлоксацин, офлоксацин, ломефлоксацин;
- 3 поколение (респираторные): левофлоксацин, спарфлоксацин, гатифлоксацин;
- 4 поколение (респираторные и антианаэробные): моксифлоксацин, гемифлоксацин.
Различия по химическим характеристикам, спектру возбудителей, во взаимодействии с организмом пациента определяет место каждого препарата в терапии.
Механизм действия препаратов обусловлен влиянием на бактериальные ферменты, участвующие в образовании ДНК и РНК. Результатом является необратимое нарушение синтеза белковых молекул микробной клетки. Падает ее жизнеспособность, уменьшается активность токсических и ферментных структур, повышается вероятность захвата бактериальной клетки фагоцитом (элементом защитной системы человека).
Фторхинолоны препятствуют делению бактериальных клеток
Представители всех групп фторхинолонов оказывают влияние на активную бактериальную клетку, а также способны нарушить любой этап ее жизненного цикла. Они действуют на растущие микроорганизмы, на клетки в состоянии покоя, когда большинство медикаментов неэффективны.
Лечебный эффект фторхинолонов обусловлен:
- бактерицидным действием;
- проникновением внутрь бактериальной клетки;
- продолжением антимикробного эффекта после прекращения контакта с молекулой препарата;
- созданием высоких концентраций в тканях, органах пациента;
- длительным выведением препарата из организма.
Налидиксовая кислота является первым представителем хинолонов. Вторым препаратом была оксолиновая кислота, обладавшая активностью в 3 раза больше предшественника. Однако, после создания фторхинолонов 2 поколения (ципрофлоксацина, норфлоксацина) это средство практически не используется.
Из хинолонов сейчас используется только налидиксовая кислота (невиграмон). Показана при инфекциях мочевых путей (пиелитах, циститах, простатите, уретрите), для предупреждения внутриоперационных осложнений на почках, мочеточнике, мочевом пузыре. Принимается до 4 раз в день (таблетки).
У фторхинолонов, как у следующего поколения хинолонов, наблюдаются изменения в спектре чувствительных микробов, а также фармакокинетических свойствах (всасывание, распределение и выведение из организма).
Общие преимущества фторхинолонов по сравнению с хинолонами:
- широкая противомикробная активность;
- эффективные концентрации во внутренних органах при применении таблетированных форм, не зависящие от приема пищи;
- хорошее проникновение в органы дыхания, почки, мочевыделительную систему, ЛОР-органы;
- для поддержания лечебных концентраций в пораженных тканях достаточно назначать 1-2 раза в сутки;
- побочные эффекты в виде нарушения деятельности органов пищеварения, нервной системы возникают реже;
- применяются при нарушенной функции почек, хотя их выведение замедляется при этой патологии.
На сегодняшний день существуют четыре генерации представителей этой группы.
Применение в клинической практике
Препараты обладают очень широким спектром, действуют на большинство микроорганизмов. Препараты 2 поколения преимущественно влияют на аэробные грам-отрицательные бактерии (сальмонеллы, шигеллы, кампилобактеры, возбудителя гонореи), грам-положительные (золотистый стафилококк, возбудитель туберкулеза).
При этом, к ним нечувствителен пневмококк, условно-патогенные микроорганизмы (хламидии, легионеллы, микоплазмы), а также анаэробы. Так как пневмококк является основным возбудителем пневмонии и часто поражает ЛОР-органы, использование этих лекарств в отоларингологии и пульмонологии имеет ограничения.
Норфлоксацин (2 генерация) обладает широким спектром воздействия, однако высокие лечебные концентрации создает только в мочевой системе. Поэтому область его применения ограничивается нефрологической, урологической патологией.
Респираторные фторхинолоны (3 поколение) имеют такой же спектр влияния, как препараты предыдущей группы, а также обладают действием на пневмококки, включая устойчивые формы, на атипичные микробы (хламидии, микоплазмы). Это позволило широко начать использовать эту группу для лечения респираторной системы (органов дыхания), а также в общетерапевтической практике.
Фторхинолоны 3 генерации применяются для лечении инфекций:
- дыхательной системы;
- почечной ткани;
- мочевыделительной системы;
- глаз;
- придаточных пазух носа;
- кожи и жировой клетчатки.
Фторхинолоны 4 генерации, последнего поколения на сегодняшний день, обладают влиянием на грам-положительную, грам-отрицательную флору, а также эффективны в отношении анаэробов, не способных к спорообразованию. Это расширяет сферу их применения, позволяет использовать при глубоких повреждениях кожи с развитием анаэробной инфекции, аспирационных пневмониях, внутрибрюшных, тазовых инфекциях.
Преимуществом современных фторхинолонов является возможность использовать только это лекарство (монотерапия).
Они показаны при тех же заболеваниях, что и респираторные фторхинолоны. При этом, москифлоксацин влияет на устойчивые штаммы стафилококков, поэтому может применяться в терапии самых тяжелых, госпитальных пневмоний.
Большим преимуществом ряда этих препаратов (левофлоксацин, пефлоксацин) является возможность их применения не только для приема внутрь, а и для внутривенного введения. Это обеспечивает быструю доставку лекарственного средства к пораженным тканям, что для тяжелых пациентов может быть решающим. Также возможно применение так называемой ступенчатой терапии. Когда при получении позитивного результата от инфузионного способа введения медикамента переходят на таблетированные формы. Высокая доступность фторхинолонов при таком способе введения обеспечивает эффективность и помогает избежать негативных последствий введения больших объемов лекарственных средств внутривенно.
Нежелательные эффекты и противопоказания к применению
Как и любые лекарственные средства, антибиотики фторхинолоны имеют ряд побочных действий. Их необходимо различать с изменениями в состоянии пациента, которые обусловлены основным заболеванием (например, временное повышение температуры тела) и указывают на терапевтический эффект медикаментов.
Перечень побочных эффектов:
- дискомфорт, боли в области желудка, снижение аппетита, изжога, тошнота, рвота, нарушения стула по типу диареи;
- нарушения сна, головные боли, головокружения, ухудшение зрения и слуха, изменение чувствительности, судорожные подергивания;
- воспаление хрящевой ткани, разрывы сухожилий;
- боли в мышцах;
- транзиторное воспаление почечной ткани, преимущественно интерстиция (нефрит);
- изменения на электрокардиограмме, в результате которых могут возникнуть аритмии;
- кожная сыпь, которая может сопровождаться зудом, аллергические отеки;
- развитие повышенной чувствительности к солнечным лучам;
- нарушения в структуре микробной флоры организма, развитие грибкового поражения слизистой оболочки рта, половых органов.
Также крайне редко, при выраженном дисбактериозе, поражении кишечника клостридиями развивается псевдомембранозный колит. Это тяжелое и опасное заболевание кишечника. Поэтому при появлении изменений стула, кровянистых или других примесей к калу, волны температуры, которую нельзя объяснить основным заболеванием, необходимо в срочном порядке проконсультироваться у врача.
- беременность на любом сроке;
- период грудного вскармливания;
- возраст менее 18 лет;
- аллергия или реакция на прием хинолонов и фторхинолонов в прошлом.
Фторхинолоны для лечения детей не используются из-за выраженного негативного влияния на хрящевую ткань растущего организма.
При необходимости эти препараты заменяют на медикаменты с подобным спектром влияния на возбудители.
При заболеваниях сердца с угрозой развития желудочковых нарушений ритма, при патологии печени и почек необходимо тщательно контролировать состояние этих органов.
У различных препаратов спектр возможного негативного влияния отличается. Поэтому применение этих средств должно проходить под строгим контролем врача.
Применение фторхинолонов при заболеваниях ЛОР-органов
При воспалительных заболеваниях носовых ходов, ротоглотки, миндалин, придаточных пазух носа, уха инфекционной природы применяют препараты пенициллинового ряда, макролиды, цефалоспорины и фторхинолоны. Используются препараты 3 и 4 поколения: левофлоксацин, моксифлоксацин, спарфлоксацин. Преимущественно средств этих генераций в том, что они влияют на пневмококки. Именно эти стрептоккоки в большинстве случаев являются возбудителями либо самостоятельно, либо совместно с другими микробами воспалительных заболеваний ЛОР-органов, дыхательной системы.
Применяют при острых и хронических воспалительных процессах, вызванных чувствительными к фторхинолонам антибиотиками.
Наиболее часто используют в терапии:
- заболеваний околоносовых пазух;
- ринитов;
- риносинуситов.
Используются фторхинолоны при отсутствии эффекта от лечения бета-лактамами (пенициллинов и цефалоспоринов) и макролидами.
Таким образом, препараты группы фторхинолонов являются одними из самых широко применяемых в современной антибактериальной терапии взрослых. Тщательное обследование пациента, выявление рисков негативного влияния, максимально точный подбор препарата под микробный спектр возбудителей конкретного заболевания, определение способа и режима введения обеспечивает позитивный эффект терапии, а также ее безопасность.
В последние годы все чаще для лечения различных инфекций применяются синтетические антибактериальные препараты. Связано это с тем, что многие микроорганизмы вырабатывают устойчивость к антибиотикам природного происхождения. Кроме того, инфекционные заболевания протекают все тяжелее, и не всегда сразу можно определить возбудителя. Поэтому возрастает потребность в антибактериальных препаратах широкого спектра действия, к которым были бы чувствительны большинство микроорганизмов. Одной из групп самых эффективных лекарств с такими свойствами являются фторхинолоны. Препараты эти получаются синтетическим путем и широко известны с 80-х годов 20 века. Клинические результаты применения этих средств доказали, что они более эффективны, чем большинство известных антибиотиков.
Антибиотики – препараты, которые обладают антимикробной активностью и чаще всего имеют природное происхождение. Формально фторхинолоны к антибиотикам не относятся. Это лекарства синтетического происхождения, полученные из хинолонов путем добавления атомов фтора. В зависимости от их количества обладают разной эффективностью и периодом выведения.
Попадая в организм, препараты группы фторхинолонов распределяются по всем тканям, попадая в жидкости, кости, проникая через плаценту и гематоэнцефалический барьер, а также в клетки бактерий. Они обладают способностью подавлять работу главного фермента микроорганизмов, без которого прекращается синтез ДНК. Это уникальное действие приводит к гибели бактерий.
Так как эти лекарства быстро распределяются по организму, они оказываются более эффективными, чем большинство других антибиотиков.
Это препараты широкого спектра действия. Считается, что они эффективны против большинства грамположительных и грамотрицательных бактерий, микоплазм, хламидий, микобактерий туберкулеза, некоторых простейших. Они уничтожают кишечную, синегнойную и гемофильную палочку, пневмококки, сальмонеллы, шигеллы, листерии, менингококки и другие. Чувствительны к ним также внутриклеточные микроорганизмы, с которыми сложно справиться другими препаратами.
Нечувствительны к этим лекарствами только разные грибки и вирусы, а также возбудители сифилиса.
Многие тяжелые и смешанные инфекции могут вылечить только фторхинолоны. Препараты, употребляемые для этого раньше, сейчас все чаще становятся неэффективными. А фторхинолоны по сравнению с ними легче переносятся пациентами, быстро всасываются, и микроорганизмы еще не могут выработать к ним устойчивость. Кроме того, лекарства этой группы имеют и другие преимущества:
- уничтожают бактерии, а не ослабляют их;
- обладают широким спектром действия;
- проникают во все органы и ткани;
- предотвращают развитие септического шока;
- могут сочетаться с другими антибактериальными препаратами;
- имеют длительный период выведения, что повышает их эффективность;
- редко вызывают побочные действия.
Антибиотики – препараты, которые вызывают множество побочных эффектов. А сейчас еще многие микроорганизмы стали нечувствительны к таким средствам. Поэтому фторхинолоны стали прекрасной альтернативой антибиотикам в лечении инфекционных заболеваний. Они обладают уникальным свойством останавливать воспроизведение клеток бактерий, что приводит к их окончательной гибели. Этим можно объяснить высокую эффективность препаратов группы фторхинолонов. К особенностям их действия относится также высокая биодоступность. Они за 2-3 часа проникают во все ткани, органы и жидкости человеческого организма. Выводятся эти препараты в основном с мочой. И намного реже, чем антибиотики, вызывают побочные действия.
Антибактериальные препараты группы фторхинолонов широко применяются при внутрибольничных инфекциях, тяжелых инфекционных заболеваниях дыхательных путей и мочеполовой системы. Даже такие серьезные инфекции, как сибирская язва, брюшной тиф, сальмонеллез, легко поддаются лечению. Ими можно заменить большинство антибиотиков. Эффективны фторхинолоны для лечения таких заболеваний:
- хламидоза;
- гонореи;
- инфекционного простатита;
- цистита;
- пиелонефрита;
- брюшного тифа;
- дизентерии;
- сальмонеллеза;
- пневмонии или хронического бронхита;
- туберкулеза.
Фторхинолоны чаще всего выпускаются в виде таблеток для приема внутрь. Но есть раствор для внутримышечного введения, а также капли в глаза и в уши. Чтобы получить нужный терапевтический эффект, необходимо соблюдать все рекомендации врача по дозировке и особенностям приема препаратов. Таблетки обязательно нужно запивать водой. Важно выдерживать необходимый интервал между приемом двух доз. Если получилось так, что один раз прием препарата пропущен, нужно принять лекарство как можно скорее, но не одновременно со следующей дозой.
При приеме препаратов группы фторхинолонов необходимо соблюдать рекомендации врача насчет сочетаемости их с другими лекарствами, ведь некоторые из них могут как снижать антибактериальный эффект, так и повышать возможность развития побочных действий. Не рекомендуется во время лечения длительное время находиться под прямыми солнечными лучами.
Сейчас наиболее безопасными бактерицидными средствами считаются фторхинолоны. Препараты эти назначаются многим категориям пациентов, которым противопоказаны другие антибиотики. Но все же определенные ограничения к их применению есть. Запрещены фторхинолоны в таких случаях:
- детям до 3 лет, а для некоторых препаратов нового поколения – до 2 лет, но в детском и подростковом возрасте они применяются только в крайних случаях;
- во время беременности и кормления грудью ребенка;
- при атеросклерозе сосудов головного мозга;
- при индивидуальной непереносимости компонентов препаратов.
При назначении фторхинолонов совместно с антицидными средствами их эффективность снижается, поэтому нужен перерыв в несколько часов между ними. Если же употреблять эти средства вместе с метилксантинами или препаратами железа, то повышается токсический эффект хинолонов.
Из всех антибактериальных средств легче всего переносятся фторхинолоны. Препараты эти могут изредка вызывать только такие побочные действия:
- боли в животе, изжогу, расстройства кишечника;
- головные боли, головокружение;
- нарушения сна;
- судороги, дрожь в мышцах;
- снижение зрения или слуха;
- тахикардию;
- нарушение функций печени или почек;
- грибковые заболевания кожи и слизистых;
- повышенную чувствительность к ультрафиолетовому облучению.
Сейчас существует четыре поколения препаратов этой группы. 
- Первое поколение – это средства с низкой эффективностью против грамположительных бактерий. К этим фторхинолонам относятся препараты, содержащие оксолиновую или налидиксовую кислоты.
- Препараты второго поколения активны против бактерий, нечувствительных к пенициллинам. Они действуют также на атипичные микроорганизмы. Часто при тяжелых инфекциях дыхательных путей и пищеварительного тракта применяются эти фторхинолоны. Препараты к этой группе относятся такие: «Ципрофлоксацин», «Офлоксацин», «Ломефлоксацин» и другие.
- Фторхинолоны 3 поколения еще называют респираторными, так как они особенно эффективны против инфекций верхних и нижних дыхательных путей. Это «Спарфлоксацин» и «Левофлоксацин».
- 4 поколение лекарств этой группы появилось недавно. Они активны против анаэробных инфекций. Пока распространен всего один препарат – «Моксифлоксацин».
Первые упоминания о препаратах этой группы можно встретить в 60-х годах 20 века. Сначала применялись против инфекций половых путей и кишечника такие фторхинолоны. Препараты, список которых известен сейчас только врачам, так как они уже почти не употребляются, обладали низкой эффективностью. Это лекарства на основе налидиксовой кислоты: «Неграм», «Невиграмон». Эти препараты первого поколения назывались хинолонами. Они вызывали много побочных действий, и многие бактерии были к ним нечувствительны.
Но исследования этих препаратов продолжились, и через 20 лет появились фторхинолоны 2 поколения. Они получили свои названия за счет введения в молекулу хинолона атомов фтора. Это повысило эффективность препаратов и уменьшило количество побочных эффектов. Ко второму поколению фторхинолонов относятся:
- «Ципрофлоксацин», известный еще под названиями «Ципробай» или «Ципринол»;
- «Норфлоксацин», или «Нолицин».
- «Офлоксацин», который можно приобрести по названием «Офлоксин» или «Таривид».
- «Пефлоксацин», или «Абактал».
- «Ломефлоксацин», или «Максаквин».
Исследования этих препаратов продолжились. И сейчас наиболее эффективными считаются современные фторхинолоны. Перечень препаратов 3 и 4 поколения еще не сильно большой, так как не все еще прошли клинические испытания и допущены к применению. Они обладают высокой эффективностью и способностью быстро проникать во все органы и ткани. Поэтому эти препараты применяются при тяжелых инфекциях дыхательных путей, мочеполовой системы, пищеварительного тракта, кожи и суставов. К ним относятся «Левофлоксацин», известный еще как «Таваник». Он эффективен даже для лечения сибирской язвы. К препаратам четвертого поколения фторхинолонов относится «Моксифлоксацин» (или «Авелокс»), который активен против анаэробных бактерий. Эти новые средства лишены большинтва недостатков остальных препаратов, легче переносятся пациентами и более эффективны.
Фторхинолоны — это одни из самых эффективных средств для лечения тяжелых инфекционных заболеваний. Но применять их можно только после назначения врача.
13. КЛИНИКО-ФАРМАКОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА ФТОРХИНОЛОНОВ
Фторхинолоны являются одной из самых распространенных и используемых групп антимикробных препаратов благодаря высокой активности в отношении широкого спектра грамотрицательных и части грамположительных возбудителей. По количеству входящих препаратов в эту группу они уступают разве что бета-лактамным
антибиотикам. Фторхинолоны—результат «чистого» химического синтеза.
Первые фторхинолоны начали использоваться в клинической
практике в начале 80-х годов прошлого столетия. Понадобилось всего четверть века, чтобы они заняли одно из ведущих мест в химиотерапии инфекций самого различного генеза и локализации.
Существует ряд классификаций, в подавляющее большинство которых включены и хинолоны. Одна из распространенных классификаций, предложеная Quintilliani R. с соавт. в 1999 году, представлена в табл. 1.
Классификация отражает, с одной стороны, генерацию, а с другой – расширение спектра антимикробного действия фторхинолонов с акцентами на менее подверженных или не склонных микробов к действию фторхинолонов предшествующих генераций.
I – нефторированные хинолоны
II – «грамотрицательные» фторхинолоны
Норфлоксацин (F=35-40%) создает высокие концентрации в ЖКТ и МВП.
Офлоксацин (F=90-95%)хуже действует на Ps.aeruginosa.
III – «респираторные» фторхинолоны
IV – респираторные» + «антианаеробные»
Фторхинолоны хорошо всасываются в ЖКТ с достижением максимума концентрации в средах организма в первые 3 ч. и циркуляцией в них в терапевтических концентрациях 5–10 ч., что позволяет их назначать 2 раза в сутки. Прием пищи замедляет всасывание, но не влияет на его полноту. Биодоступность фторхинолонов при приеме внутрь достигает 80–100 %. Исключением является только норфлоксацин с биодоступностью 35–40 %. Фторхинолоны хорошо проникают в различные ткани организма, создавая концентрации близкие к сывороточным или превышающие их. Это обусловлено их физико-химическими свойствами: высокой липофильностью и низким связыванием с белками. В тканях ЖКТ, мочеполовых и дыхательных путей, почек, синовиальной жидкости их концентрация составляет более 150 % по отношению к сывороточной, показатель проникновения фторхинолонов в мокроту, кожу, мышцы, матку, воспалительную жидкость и слюну составляет 50–150 %, а в спинно-мозговую жидкость, жир и ткани глаза – менее 50 %.
Фторхинолоны хорошо проникают не только в клетки человеческого организма (полиморфноядерные нейтрофилы, макрофаги, альвеолярные макрофаги), но и в клетки микроорганизмов, что имеет важное значение при лечении инфекций с внутриклеточной локализацией микробов.
Элиминация фторхинолонов в организме осуществляется почечным и внепочечным (биотрансформация в печени, экскреция с желчью, выведение с фекалиями и др.) путем. Почти полностью почечным путем выводится офлоксацин и ломефлоксацин, преимущественно внепочечными механизмами – пефлоксацин и спарфлоксацин; другие препараты занимают промежуточное положение.
В основе механизма действия фторхинолонов лежит угнетение ДНК-гиразы или топоизомеразы IV микробов, что объясняет отсутствие перекрестной резистентности с другими классами антимикробных препаратов. Резистентность к фторхинолонам развивается относительно медленно. Она связана с мутациями генов, кодирующих ДНК-гиразу или топоизомеразу IV, а также с нарушением их транспорта через пориновые каналы во внешней клеточной мембране микроба или выведением из него путем активации белков выброса.
Спектр антимикробного действия
Спектр антимикробного действия фторхинолонов охватывает аэробных и анаэробных бактерий, микобактерии, хламидии, микоплазмы, риккетсии, борелии и некоторые простейшие.
I – нефторированные хинолоны
Грамм (–) микрофлора (семейство Enterobacteriaceae)
II – «грамотрицательные» фторхинолоны
Грамм (–) микрофлора, S. aureus, низкая активность против Streptococcus pneumoniaе, Mycoplasma pneumoniae, Chlamydophila pneumoniae
III – «респираторные» фторхинолоны
Активность против Streptococcus pneumoniae, Mycoplasma pneumoniae, Chlamydophila pneumoniae
IV – респираторные» + «антианаеробные»
Активность против Streptococcus pneumoniae, Mycoplasma pneumoniae, Chlamydophila pneumoniae, неспорообразующие анаэробов
Фторхинолоны имеют естественную активность в отношении грамотрицательных бактерий семейств Enterobacteriaceae (Citrobacter, Enterobacter, Escherichia coli, Klebsiella, Proteus, Providencia, Salmonella, Shigella, Yersinia), Neisseriae (gonorrhoeae, meningitidis), Haemophilus и Moraxella, высокоактивны в отношении легионелл, микоплазм и хламидий, а также проявляют, хотя и меньшую, активность к неферментирующим грамотрицательным бактериям, грамположительным коккам, микобактериям и анаэробам. Разные фторхинолоны по-разному действуют как на разные группы, так и отдельные виды микробов.
К фторхинолонам II поколения малочувствительны большинство стрептококков (в частности пневмококк), энтерококки, хламидии, микоплазмы. Не действуют они на спирохеты, листерии и большинство анаэробов.
Фторхинолоны III поколения по сравнению со II поколением обладают более высокой активностью к пневмококкам (включая пенициллинорезистентные) и атипичным возбудителям (хламидии, микоплазмы).
Фторхинолоны IV поколения по антипневмококковой активности и действию на атипичных возбудителей превосходят препараты предшествующих поколений, показывая также высокую активность против неспорообразующих анаэробов, благодаря чему применяются также при интраабдоминальных и тазовых инфекциях, причем даже в виде монотерапии.
Показания по использованию в клинической практике
– Инфекции мочевыводящих путей: острый цистит, противорецидивная терапия при хронических формах инфекций (не следует применять при остром пиелонефрите).
– Кишечные инфекции: шигеллез, бактериальные энтероколиты (налидиксовая кислота).
– Инфекции верхних дыхательных путей: синусит, особенно вызванный полирезистентнымы штаммами, злокачественный наружный отит.
– Инфекции нижних дыхательных путей: обострение хронического бронхита, внебольничная и нозокомиальная пневмония, легионеллез.
– Кишечные инфекции: шигеллез, брюшной тиф, генерализованный сальмонеллез, иерсиниоз, холера.
– Инфекции органов малого таза.
– Инфекции мочевыводящих путей (цистит, пиелонефрит).
– Инфекции кожи, мягких тканей, костей и суставов.
– Менингит, вызванный грамотрицательной микрофлорой (ципрофлоксацин).
– Бактериальные инфекции у пациентов с муковисцидозом.
– Туберкулез (ципрофлоксацин, офлоксацин и ломефлоксацин в комбинированной терапии при лекарственноустойчивом туберкулезе).
Норфлоксацин, с учетом особенностей фармакокинетики, применяется только при кишечных инфекциях, инфекциях мочевыводящих путей и простатите.
Важное преимущество фторхинолонов – высокая эффективность монотерапии инфекций, вызванных широким спектром аэробных грамотрицательных бактерий и возбудителями с внутриклеточной локализацией. Однако при микобактериозах, аэробно-анаэробных и стрептококковых (из стрептококков различных групп) инфекциях их необходимо использовать только в схемах комбинированной терапии.
Следует помнить, что фторхинолоны не показаны при энтерококковой инфекции, протозойных заболеваниях, микозах, вирусной инфекции, сифилисе и некоторых других состояниях.
Фторхинолоны II поколения из-за невысокой природной активности к грамположительным микробам, прежде всего Streptococcus pneumoniae, не рекомендуются для лечения внебольничных респираторных инфекций. Напротив, фторхинолоны III и IV поколений помимо высокой антимикробной активности характеризуются свободным проникновением в неклеточные и клеточные структуры дыхательных путей, благодаря чему их концентрации здесь оказываются выше, чем в сыворотке крови, что
позволило рекомендовать их для лечения респираторных инфекций.
Фторхинолоны III и IV поколений имеют бактерицидную активность
с постантибиотическим действием и характеризуются длительной циркуляцией в организме с большим периодом полувыведения. Благодаря этому они назначаются всего 1 раз в сутки, что весьма удобно на практике.
В концентрации 1-5мкг/мл действует на грамм (–) микрофлору (семейство Enterobacteriaceae, Ps.aeruginosa, нейссерии. В концентрации более 5 мкг/мл подавляет грамм (+) микрофлору и внутриклеточные паразиты (легионеллы, хламидии, микоплазмы).
Взрослые: 0,5–1,0 г каждые 6 ч.
Дети старше 3 мес.: 55 мг/кг в сут. в 4 приема
0,2 г) во флак. по 50 мл и 100 мл.
капли 0,3 % во флаконах-капельницах по 5 и 10мл.
Мазь для глаз 0,3 % в тюбиках по 3 и 5 г.
Внутрь (не разжевывая, запивая водой).
Взрослые: 0,25–0,75 г каждые 12 ч.;
при остром цистите у женщин – до 0,5 г каждые 12 ч. в течение 7-14 дней;
при острой гонорее – 0,5 г однократно.
Взрослые: 0,4–0,6 г каждые 12 ч.
Вводят путем медленной инфузии в течение 1 ч.
Капли для глаз: закапывают по 1–2 кап. в пораженный глаз каждые 4 ч., при тяжелом течение – каждый час до улучшения.
Ушные капли закапывают по 2–3 кап. в пораженное ухо 4–6 раз в сут., при тяжелом течение – каждые 2–3 ч., постепенно уменьшая до улучшения.
Мазь для глаз закладывают за нижнее веко пораженного глаза 3-5 раз в сут.
Внутрь (не разжевывая, запивая водой).
Взрослые: 0,25–0,5 г каждые 12–24 ч.; при пневмонии и тяжелых формах инфекций – 0,5 г каждые 12 ч до 14 дней.
Взрослые: 0,25–0,5 г каждые 12–24 ч. Вводят путем медленной инфузии в течение 1 ч.
Фторхинолоны в большинстве случаев хорошо переносятся как при приеме внутрь, так и внутривенном введении. Побочные эффекты наблюдаются редко, но если возникают, то чаще со стороны пищеварительного тракта и центральной нервной системы.
В первом случае это тошнота, рвота, диарея, изжога, боль, нарушения
вкуса, запоры, диспепсия, глоссит, стоматит, кандидоз и другие. Во втором – головокружение, головная боль, нарушение сна, парестезии, тремор, судороги, нарушения слуха, нервозность, сновидения.
Опасные побочные эффекты, проявление которых требует отмены препарата:
1) Эпилепсия, судороги (особенно на фоне приёма НПВС)
2) На основании экспериментальных данных на животных применения хинолонов не рекомендуется в период формирования костно-суставной системы (торможение развития хрящевой ткани).Оксолиновая кислота противопоказана детям до 2 лет, пипемидовая – до 1 года, налидиксовая – до 3 мес.
3) Тендиниты (есть сообщения об отдельных случаях разрыва сухожилий скелетных мышц (главным образом это касается пожилых пациентов, принимающих стероидные препараты)).
4) Риск фотосенсибилизации.
5) Удлинение интервала QT—риск желудочковых аритмий
6) Возможны аллергические реакции в виде зуда, сыпи, ангио-невротического отека.
У пациентов с нарушениями углеводного обмена, прежде всего с сахарным диабетом, при почечной недостаточности, а также у лиц старческого возраста вместо фторхинолонов IV поколения рекомендуется использовать антимикробные препараты других групп.
– Аллергическая реакция на препараты группы хинолонов. Перекрестная ко всем препаратам группы хинолонов.
Дополнительно для хинолонов I поколения:
– Тяжелые нарушения функции печени и почек.
– Тяжелый церебральный атеросклероз.
Дополнительно для всех фторхинолонов:
– Кормление грудью. В небольших количествах хинолоны проникают в грудное молоко. По некоторым данным, они могут вызвать гемолитическую анемию у новорожденных, матери которых принимали налидиксовую кислоту в период кормления грудью. Поэтому кормящим матерям на период лечения хинолонами рекомендуется перевести ребенка на искусственное вскармливание.
Фторхинолоны не рекомендуется назначать детям и подросткам.
Допускается назначение детям только по жизненным показаниям (обострение инфекции при муковисцидозе; тяжелые инфекции различной локализации, вызванные полирезистентнимы штаммами бактерий;
Заболевания ЦНС. Хинолоны возбуждают ЦНС и их не рекомендуют применять пациентам с судорожным синдромом в анамнезе.
При использовании налидиксовой кислоты возможно повышение внутричерепного давления.
Нарушение функции почек и печени. Хинолоны I поколения нельзя применять при почечной и печеночной недостаточности, поскольку вследствие кумуляции препаратов и их метаболитов повышается риск токсических эффектов. Дозы фторхинолонов при тяжелой почечной недостаточности подлежат коррекции.
При одновременном применении с антацидами и другими препаратами, содержащими ионы магния, цинка, железа, висмута, может снижаться биодоступность хинолонов вследствие образования невсасывающихся хелатных комплексов.
Пипемидовая кислота, ципрофлоксацин, норфлоксацин и пефлоксацин могут замедлять элиминацию метилксантинов (теофиллин, кофеин) и повышать риск их токсических эффектов.
Риск нейротоксических эффектов хинолонов повышается при совместном применении с НПВС, производными нитроимидазола и метилксантинами.
Хинолоны проявляют антагонизм с производными нитрофурана, поэтому следует избегать комбинаций с этими препаратами.
Хинолоны I поколения, ципрофлоксацин и норфлоксацин могут нарушать метаболизм непрямых антикоагулянтов в печени, что приводит к увеличению протромбинового времени и риска кровотечений. При одновременном применении может потребоваться коррекция дозы антикоагулянта.
Следует с осторожностью назначать фторхинолоны одновременно с препаратами, которые удлиняют интервал QT, поскольку увеличивается риск развития сердечных аритмий.
При одновременном применении с ГКС повышается риск разрыва сухожилий, особенно у пожилых людей.
При использовании ципрофлоксацина, норфлоксацина и пефлоксацин совместно с препаратами, ощелачивающими мочу (ингибиторы карбоангидразы, цитраты, натрия бикарбонат), увеличивается риск кристаллурии и нефротоксических эффектов.
Зачем нужны антибиотики в наше время, знает даже школьник. Но словосочетание «широкий спектр» порой вызывает вопросы у пациентов. Почему именно «широкий»? Возможно, меньше вреда будет от антибиотика с «узким» спектром?
Бактерии – это очень древние, чаще всего одноклеточные, безъядерные микроорганизмы, живущие в почве, воде, человеке и животных. В человеческом организме живут «хорошие» бифидо- и лактобактерии, эти бактерии формируют микрофлору человека.
Вместе с ними существуют и другие микроорганизмы, они называются условно патогенными. При болезнях и стрессах иммунная система дает сбой и эти бактерии становятся совсем недружелюбными. И конечно же, в организм попадают различные микробы, вызывающие заболевания.
Ученые разделили бактерии на две группы, грамположительные (Грамм +) и грамотрицательные (Грамм -). Коринебактерии, стафилококки, листерии, стрептококки, энтерококки, клостридии, относятся к грамположительной группе бактерий. Возбудители этой группы, как правило, являются причиной заболеваний уха, глаз, бронхов, легких, носоглотки и т.п.
Грамотрицательные бактерии негативно влияют на кишечник и мочеполовую систему. К таким возбудителям относятся кишечная палочка, моракселла, сальмонелла, клебсиелла, шигелла и др.
На основании такого бактериального разделения для лечения заболеваний, вызванных определенными возбудителями, назначается антибактериальная терапия. Если заболевание «стандартное» или же имеется результат бактериального посева, врач назначает антибиотик, который справится с возбудителями, принадлежащими к одной из групп. Когда времени на проведения анализа нет и врач сомневается в принадлежности возбудителя, тогда для лечения назначают антибиотики, имеющие более широкий спектр действия. Эти антибиотики бактерицидно действуют в отношении большого числа возбудителей.
Такие антибиотики разделяют на группы. Одной из них является группа фторхинолонов.
Препараты класса хинолонов во врачебной практике стали применять еще с начала 60-х годов прошлого века. Делятся хинолоны на нефторированные хинолоны и фторхинолоны.
- Нефторированные хинолоны оказывают антибактериальное действие в основном на грамотрицательную группу бактерий.
- У фторхинолонов ширина спектра действия намного больше. Помимо влияния на ряд Грамм- бактерий, фторхинолоны с успехом борются и с грамположительной группой бактерий. Антибиотики фторхинолоны показывают высокий бактерицидный эффект, благодаря этому были разработаны и медицинские препараты для местного применения (капли, мази), которые используются при лечении болезней ушей и глаз.
Четыре поколения препаратов
- 1 поколение хинолонов называют нефторированными хинолонами. Оно состоит из оксолиновой, налидиксовой и пипемидовой кислот. Например, на основе налидиксовой кислоты выпускаются препараты уроантисептики Неграм и Невиграмон. Эти антибиотики действуют бактерицидно в отношении сальмонеллы, клебсиеллы, шигеллы, но плохо справляются с анаэробными бактериями и Грам+ бактериями.
- 2 поколение лечебных препаратов фторхинолонового ряда состоит из следующих антибиотиков: норфлоксацин, ломефлоксацин, офлоксацин, пефлоксацин, а также ципрофлоксацин. При введении атомов фтора в молекулы хинолона последние стали называться фторхинолонами. Фторхинолоны 2 поколения хорошо борются с большим количеством Грам- кокков и палочек (шигелла, сальмонелла, гонококки и др.). С грамположительными палочками (листерии, коринебактериии и др.), легионеллой, стафилоккоком и др. Ципрофлоксацин, ломефлоксацин и офлоксацин подавляют увеличение микобактерий, вызывающих туберкулез, но при этом проявляют малую активность в борьбе с пневмококками, хламидиями, микоплазмами и анаэробными бактериями.
Названия препаратов, имеющих в составе фторхинолоны 2 поколения
- Ципрофлоксацин (Ципролет, Флоксимет) назначается для лечения отитов, синуситов. При болезнях органов мочеполовой системы – цистит, простата, пиелонефрит. Для лечения болезней ЖКТ, например, бактериальная диарея. В гинекологии — аднексит, эндометрит, сальпингит, абсцесс малого таза. При гнойном артрите, холецистите, перитоните, гонорее и др. В каплевой форме применяется при болезнях глаз, таких как кераконъюнктивит и кератит, блефарит и др.
- Пефлоксацин (Перти, Абактал, Юникпеф) назначается для лечения инфекций мочевыводящей системы. Актуален для лечения тяжелых форм болезней ЖКТ, например, сальмонеллез. Эффективен при бактериальном простатите и гонореи. Применяется при лечении пациентов, у которых нарушен иммунный статус. Используется для лечения болезней носоглотки, горла, нижних дыхательных путей и др. Лучше других фторхинолонов проходит через физиологический барьер между кровеносной и центральной нервной системами.
- Офлоксацин (Унифлокс, Флоксал, Заноцин) лечит синусит и отит. Активно ведет себя в отношении бактерий, вызывающих заболевания мочевыводящих путей. Применим при лечении гонореи, хламидиоза, менингита. При местном лечении капельной формой антибиотика или мазью лечат болезни глаз, такие как ячмень, язва роговицы, конъюнктивит и др. Среди антибиотиков 2 поколения Офлоксацин эффективнее всего справляется с пневмококками и хламидиями.
- Ломефлоксацин (Ломфлокс, Ломацин). К препарату имеют устойчивость некоторые группы стрептококка и анаэробные бактерии, зато этот антибиотик обладает высокой активностью к большому количеству микроорганизмов даже в самых маленьких концентрациях. Применяется для лечения больных туберкулезом в составе комплексной терапии. Назначается для лечения болезней мочеполовой системы, для местного применения при лечении заболеваний в офтальмологии и др. Имеет малую активность в борьбе с пневмококками, микоплазмами и хламидиями.
- Норфлоксацин (Норбактин, Нормакс, Норфлогексал) применятся при лечении болезней в офтольмологии, урологии, гинекологии и др.
3 поколение фторхинолонов
3 поколение фторхинолонов называют также респираторными фторхинолонами. Эти антибиотики имеют такой же большой спектр влияния, как фторхинолоны предыдущего поколения, а также превосходят оных в борьбе с пневмококками, хламидиями, микоплазмами и другими возбудителями респираторных инфекций. Благодаря этому 3 поколение препаратов фторхинолонового ряда часто используется для лечения болезней дыхательной системы.
Названия препаратов, имеющих в составе фторхинолоны 3 поколения
- Левофлоксацин (Флорацид, Левостар, Леволет Р) в 2 раза сильнее действует в отношении бактерий, чем его предшественник 2 поколения офлоксацин. Применяется при лечении инфекций нижней дыхательной системы и Лор-органов (отит, синусит). Назначается при болезнях мочеполового тракта, хроническом простатите, заболеваниях, передающихся половым путем, при лечении острого пиелонефрита. В виде капель данный антибиотик используют в офтольмологии при глазных инфекциях. Лучше переносится, чем антибиотик 2 поколения офлоксацин.
- Спарфлоксацин (Спарфло, Спарбакт) по широте спектра активности этот антибиотик ближе всего к Левофлоксацину. Имеет высокую эффективность в борьбе с микобактериями. Длительность действия выше, чем у других фторхинолонов. Используется для борьбы с бактериями в придаточных пазухах носа, среднем ухе. При лечении болезней почек, половой системы, бактериальном поражении кожи и мягких тканей, инфекций ЖКТ, костей, суставов и др.
4 поколение препаратов фторхинолонового ряда включают в себя следующие наиболее известные препараты: моксифлоксацин, гемифлоксацин, гатифлоксацин.
Медицинские препараты, имеющие в составе фторхинолоны 4 поколения
- Гемифлоксацин (Фактив) используется при лечении пневмонии, хронического бронхита, синусита и др.
- Гатифлоксацин (Зимар, Гатиспан, Зарквин). Биодоступность этого антибиотика очень высока, порядка 96%, при пероральном приеме. В легочной ткани, среднем ухе, оболочке бронхов, сперме, слизистой придаточных пазух, яичниках фиксируются довольно большие концентрации. Назначается для лечения болезней Лор-органов, заболеваний, передающихся половым путем, болезней кожи и суставов. Препарат используют для лечения бронхитов, пневмонии, кистозного фиброза, бактериальных конъюнктивитов и других болезней, вызванных чувствительными к антибиотику бактериями.
- Моксифлоксацин (Авелокс, Вигамокс). Исследования инвитро показали, что этот антибиотик лучше других фторхинолонов справляется с лечением инфекций, которые вызваны пневмококками, хламидиями, микоплазмами, анаэробами. Назначается врачами при бронхитах, пневмонии, синуситах, инфекционных поражениях кожи, мягких тканей. Лечит воспаления органов малого таза. В виде жидкости применяется в офтольмотологии при местном лечении ячменя, конъюнктевита, блефарита, язвы роговицы. Превосходство этого фторхинолона последнего поколения над предыдущими поколениями определяется и его фармакокинетическими свойствами:
- Высокие бактерицидные концентрации в различных органах и тканях, обеспечиваются его хорошей проникаемостью.
- Антибиотик можно применять до одного раза в день из-за его долгой циркуляции в организме.
- На всасываемость данного фторхинолона не влияет прием пищи.
- Абсолютная биодоступность препарата после перорального приема составляет от 85% до 93%.
Несколько препаратов фторхинолонового ряда, а именно моксифлоксацин, гатифлоксацин, ципрофлоксацин, ломефлоксацин, левофлоксацин, офлоксацин, спарфлоксацин вошли в список жизненно необходимых и важнейших лекарственных препаратов, утвержденный Правительством РФ.
источник







