Основное клиническое значение аминогликозидов заключается в их активности в отношении грамотрицательных бактерий. Аминогликозиды обладают более быстрым, чем β-лактамы, бактерицидным действием, очень редко вызывают аллергические реакции, но по сравнению с β-лактамами значительно более токсичны. Классифицируются аминогликозиды по поколениям (табл. 4).
| Грам(+) кокки: | стафилококки, включая PRSA и некоторые MRSA (аминогликозиды II-III поколений); стрептококки и энтерококки умеренно чувствительны к стрептомицину и гентамицину. |
| Грам(-) кокки: | гонококки, менингококки — умеренно чувствительны. |
| Грам(-) палочки: | E.coli, протеи (аминогликозиды I-III поколений), клебсиеллы, энтеробактеры, серрации (аминогликозиды II-III поколений); P.aeruginosa (аминогликозиды II-III поколений). |
| Микобактерии: | M.tuberculosis (стрептомицин, канамицин и амикацин). |
| Анаэробы устойчивы. | |
А. Пневмококки устойчивы к аминогликозидам, поэтому ошибкой является их применение при внебольничной пневмонии.
Б. Стрептококки, включая группу зеленящих стрептококков, в целом малочувствительны к аминогликозидам. Но при применении совместно с пенициллином отмечается выраженный синергизм. Поэтому при лечении, например, бактериального эндокардита, используют сочетание бензилпенициллина (или ампициллина) с гентамицином (или стрептомицином).
В. Несмотря на то, что сальмонеллы и шигеллы in vitro чувствительны к аминогликозидам, для лечения шигеллеза и сальмонеллеза эти антибиотики нельзя применять в связи с низкой эффективностью. Это обусловлено плохим проникновением аминогликозидов внутрь клеток человека, где локализуются шигеллы и сальмонеллы. Чтобы избежать ненужных исследований и не вводить клиницистов в заблуждение при интерпретации результатов определения чувствительности, не рекомендуется определять чувствительность к аминогликозидам шигелл и сальмонелл.
Практически не всасываются в ЖКТ (перорально назначаются для селективной деконтаминации ЖКТ перед операциями на толстом кишечнике или у пациентов, находящихся в ОРИТ). Хорошо всасываются при введении внутримышечно, интраперитонеально и интраплеврально. По сравнению с β-лактамами и фторхинолонами хуже проходят через различные тканевые барьеры (ГЭБ, ГОБ), создают более низкие концентрации в бронхиальном секрете, желчи. Высокие уровни отмечаются в ткани почек. В печени не метаболизируются, выводятся с мочой в неизмененном виде. Т1/2 всех препаратов — 2-3,5 ч. У новорожденных в связи с незрелостью почек Т1/2 возрастает до 5-8 ч.
- Пожилой возраст.
- Высокие дозы.
- Длительное применение (более 7-10 дней).
- Гипокалиемия.
- Дегидратация.
- Поражения вестибулярного и слухового аппарата.
- Почечная недостаточность.
- Одновременный прием других нефротоксичных и ототоксичных препаратов (амфотерицин В, полимиксин В, фуросемид и др.).
- Одновременное введение с миорелаксантами.
- Миастения.
- Быстрое внутривенное введение аминогликозидов или их больших доз в брюшную и плевральную полость.
- Не превышать максимальные суточные дозы, если нет возможности определять концентрацию аминогликозидов в крови.
- Контролировать функцию почек до назначения аминогликозидов и затем каждые 2-3 дня путём определения креатинина сыворотки крови с расчетом клириенса креатинина.
- Соблюдать максимальную продолжительность терапии — 7-10 дней, исключение составляют бактериальный эндокардит — до 14 дней, туберкулёз — до 2 мес.
- Нельзя назначать одновременно два аминогликозида или заменять один препарат другим, если первый аминогликозид применялся в течение 7-10 дней. Повторный курс можно проводить не ранее чем через 4-6 недель.
- Контролировать слух и вестибулярный аппарат (опрос пациентов, при необходимости аудиометрия).
Прежде всего — отмена препарата. Нарушения слуха, как правило, бывают необратимыми, тогда как функция почек постепенно восстанавливается. При развитии нервно-мышечной блокады как антидот внутривенно вводят кальция хлорид.
Синергизм при сочетании с пенициллинами или цефалоспоринами (но не при введении в одном шприце!).
Антагонизм с β-лактамными антибиотиками и гепарином при смешивании в одном шприце вследствие физико-химической несовместимости.
Усиление токсических эффектов при сочетании с другими нефротоксичными и ототоксичными препаратами (полимиксин В, амфотерицин В, фуросемид и др.).
- Инфекции различной локализации, вызванные грамотрицательными бактериями из семейства Enterobacteriaceae (кишечная палочка, клебсиеллы, энтеробактеры и др.) и неферментирующими бактериями (ацинетобактеры, S.maltophilia и др.) — аминогликозиды II-III поколений.
- Синегнойная инфекция — аминогликозиды II-III поколений.
- Энтерококковые инфекции — гентамицин или стрептомицин обязательно в сочетании с пенициллином или ампициллином.
- Туберкулёз — стрептомицин, канамицин, амикацин — обязательно в сочетании с другими противотуберкулёзными препаратами.
- Зоонозные инфекции: чума, бруцеллез (стрептомицин); туляремия (стрептомицин, гентамицин).
Ввиду того, что при применении аминогликозидов могут развиваться тяжёлые нежелательные реакции, а также учитывая особенности их фармакокинетики (выведение через почки в неизмененном виде), особое внимание следует уделять правильному расчету доз аминогликозидов. При этом следует принимать во внимание два ключевых положения:
- доза аминогликозидов (не только у детей, но и у взрослых!) должна рассчитываться, исходя из массы тела;
- доза должна быть скорригирована исходя из индивидуальных особенностей пациента: возраст, функция почек, локализация инфекции.
| 1. | Масса тела пациента Дозы у взрослых и детей старше 1 мес: стрептомицин, канамицин, амикацин — 15-20 мг/кг/сут в 1-2 введения; гентамицин, тобрамицин — 3-5 мг/кг/сут в 1-2 введения; нетилмицин — 4-6,5 мг/кг/сут в 1-2 введения. |
| 2. | Ожирение/истощение Так как аминогликозиды распределяются во внеклеточной жидкости и не накапливаются в жировой ткани, их дозы при ожирении следует уменьшать. В случае превышения идеальной массы тела на 25% и более дозу, рассчитанную на фактическую массу тела, следует снизить на 25%. У истощённых пациентов дозу, наоборот, следует увеличить на 25%. |
| 3. | Возраст Необходимо уменьшать дозу аминогликозидов у пожилых, так как у них отмечается возрастное снижение клубочковой фильтрации. Новорожденные дети должны получать относительно большую на кг массы тела дозу, поскольку у них увеличен объем распределения. Так, доза гентамицина составляет у них до 7,5 мг/кг/сут. В целом у новорожденных доза аминогликозидов и кратность введения зависят от двух факторов: степени недоношенности и постнатального возраста. Это связано с незрелостью функции почек, становление которой происходит после рождения. |
| 4. | Функция почек Поскольку аминогликозиды выделяются из организма в неизмененном виде с мочой, при нарушении функции почек необходимо снижать суточную дозу. Наиболее информативный показатель функции почек — клиренс эндогенного креатинина (клубочковая фильтрация), который рассчитывается у взрослых по формуле Кокрофта и Голта (Cockroft, Gault, 1976), а у детей по формуле Шварца (Schwarz, 1987). Для правильного выбора дозы аминогликозидов определение креатинина сыворотки крови и расчет его клиренса необходимо проводить перед назначением препарата и повторять каждые 2-3 дня. |
Cнижение клиренса креатинина более чем на 25% от исходного уровня свидетельствует о возможном нефротоксическом действии аминогликозидов, уменьшение более чем на 50% — является показанием для отмены аминогликозидов.
При почечной недостаточности первая разовая доза гентамицина, тобрамицина и нетилмицина составляет 1,5-2 мг/кг, амикацина — 7,5 мг/кг. Последующие разовые дозы определяются по формуле:
| 1-я доза (мг) × КК 100 |
- где КК — клиренс креатинина в мл/мин/1,73 м 2 .
При менингите, пневмонии, сепсисе назначают максимальные дозы; при пиелонефрите, бактериальном эндокардите — средние дозы. Особенно высокие дозы вводят пациентам с муковисцидозом и при ожогах, так как у них значительно нарушено распределение аминогликозидов, но при этом желательно определять концентрацию аминогликозидов в крови.
Традиционно аминогликозиды вводились 2-3 раза в сутки. Однако в результате многочисленных исследований было показано, что во многих случаях всю суточную дозу аминогликозидов можно вводить один раз в сутки. При однократном режиме введения клиническая эффективность не снижается, а частота нежелательных реакций даже может уменьшаться.
Однократное введение применяется при большинстве показаний. Исключение составляют эндокардит, менингит, период новорожденности.
При однократном введении аминогликозиды лучше всего вводить внутривенно капельно в течение 15-20 мин, так как внутримышечно трудно ввести большой объем препарата.
Для аминогликозидов установлена взаимосвязь между их концентрацией в крови, антимикробным эффектом и частотой развития ототоксичности и нефротоксичности. В то же время фармакокинетика аминогликозидов имеет большие индивидуальные колебания. Вследствие этого при введении средних доз препаратов примерно у половины пациентов отмечаются субтерапевтические концентрации.
| Препарат | Концентрация, мкг/мл | |
|---|---|---|
| пиковая, не менее | остаточная, не более | |
| Гентамицин | 6-10 | 2 |
| Тобрамицин | 6-10 | 2 |
| Нетилмицин | 6-10 | 2 |
| Амикацин | 20-30 | 10 |
При проведении терапевтического лекарственного мониторинга определяют:
| 1) | пиковую концентрацию аминогликозидов в сыворотке крови — через 60 мин после внутримышечного введения препарата или через 15 мин после окончания внутривенного введения; |
| 2) | остаточную концентрацию — перед введением очередной дозы. |
Установление пиковой концентрации не ниже порогового значения (табл. 5) свидетельствует о достаточности используемой дозы аминогликозида, при этом ее высокие уровни не представляют опасности для пациента. Величина остаточной концентрации, превышающая терапевтический уровень, свидетельствует о кумуляции препарата и об опасности развития токсических эффектов. В этом случае снижают суточную дозу или удлиняют интервал между разовыми дозами. При однократном введении всей суточной дозы достаточно определять только остаточную концентрацию.
Первый аминогликозидный антибиотик. Обладает высокой кохлеатоксичностью и особенно вестибулотоксичностью, но является наименее нефротоксичным из аминогликозидов. К нему быстро развивается устойчивость микрофлоры.
В настоящее время ограничены следующими заболеваниями:
- туберкулёз;
- бактериальный эндокардит, вызванный зеленящими стрептококками или энтерококками (в сочетании с пенициллином или ампициллином);
- бруцеллёз, туляремия, чума (в комбинации с тетрациклином).
Парентерально — 15 мг/кг/сут (не более 2,0 г/сут) в 1-2 введения.
Внутримышечно — по 1,0 г 2 раза в неделю.
Внутримышечно — 20 мг/кг/сут 2 раза в неделю.
Флаконы по 0,25 г, 0,5 г, 1,0 г и 2,0 г порошка для приготовления раствора для инъекций.
Один из наиболее ототоксичных препаратов. Парентеральное введение его запрещено. Иногда используется внутрь для селективной деконтаминации ЖКТ перед операциями на толстом кишечнике и местно (входит в состав некоторых мазей в сочетании с глюкокортикоидами). У детей не применяют.
Внутрь — по 0,5 г каждые 6 ч в течение 1-2 дней.
Таблетки по 0,1 г и 0,25 г; 0,5% и 2% мазь.
Устаревший препарат. В отличие от аминогликозидов II поколения действует на M.tuberculosis, но уступает им и амикацину по активности в отношении нозокомиальных штаммов грамотрицательной флоры. Не действует на синегнойную палочку.
Обладает высокой ототоксичностью и нефротоксичностью.
Сохраняет свое значение при туберкулёзе как препарат II ряда. Внутрь может применяться по тем же показаниям, что и неомицин.
Внутрь — по 2-3 г каждые 6 ч; парентерально — 15 мг/кг/сут в 1-2 введения.
Парентерально — 15 мг/кг/сут в 1-2 введения.
Таблетки по 0,125 г и 0,25 г; флаконы по 0,5 г и 1,0 г порошка для приготовления раствора для инъекций.
Основной аминогликозид II поколения. Действует на синегнойную палочку.
По сравнению со стрептомицином более нефротоксичен, но менее ототоксичен.
- Нозокомиальная пневмония (при низком уровне резистентности).
- Инфекции МВП.
- Интраабдоминальные и тазовые инфекции (в сочетании с антианаэробными препаратами).
- Бактериальный эндокардит (в сочетании с пенициллином или ампициллином).
- Сепсис (в сочетании с β-лактамами).
- Туляремия.
В настоящее время в связи с широким (часто необоснованно) использованием гентамицина многие нозокомиальные микроорганизмы, прежде всего синегнойная палочка и клебсиелла, приобрели резистентность к препарату.
Грубой ошибкой является применение гентамицина при внебольничной пневмонии, так как гентамицин, как и другие аминогликозиды, не действует на пневмококки.
Парентерально — 3-5 мг/кг/сут в 1-2 введения.
Парентерально — 5-7,5 мг/кг/сут в 2-3 введения.
Флаконы по 0,08 г порошка для приготовления раствора для инъекций; ампулы по 1 мл и 2 мл 4% раствора (40 мг/мл); 0,1% мазь.
По сравнению с гентамицином более активен в отношении синегнойной палочки, однако в большинстве случаев отмечается ко-резистентность к обоим препаратам. Не действует на энтерококки. Менее нефротоксичен.
- Нозокомиальная пневмония.
- Инфекции МВП.
- Интраабдоминальные и тазовые инфекции (в сочетании с антианаэробными препаратами).
- Сепсис (в сочетании с β-лактамами).
Парентерально — 3-5 мг/кг/сут в 1-2 введения.
Ампулы по 1 мл и 2 мл 4% раствора (40 мг/мл).
Активен против некоторых нозокомиальных штаммов грамотрицательных бактерий, устойчивых к гентамицину. По сравнению с гентамицином обладает несколько меньшей ототоксичностью и нефротоксичностью.
- Нозокомиальная пневмония.
- Инфекции МВП.
- Интраабдоминальные и тазовые инфекции (в сочетании с антианаэробными препаратами).
- Бактериальный эндокардит (в сочетании с цефтриаксоном).
- Сепсис (в сочетании с β-лактамами).
Парентерально — 4-6,5 мг/кг/сут в 1-2 введения.
Раствор для инъекций во флаконах по 2 мл, содержащих 0,05 г или 0,15 г нетилмицина.
Действует на многие штаммы грамотрицательных бактерий (в том числе P.aeruginosa), резистентные к гентамицину и другим аминогликозидам II поколения. Активен против M.tuberculosis. Не действует на энтерококки.
По сравнению с гентамицином несколько менее нефротоксичен.
Используется для лечения инфекций, вызванных полирезистентной грамотрицательной микрофлорой. Наиболее предпочтителен среди аминогликозидов для эмпирической терапии нозокомиальных инфекций.
- Нозокомиальная пневмония.
- Инфекции МВП.
- Интраабдоминальные и тазовые инфекции (в сочетании с антианаэробными препаратами).
- Сепсис (в сочетании с β-лактамами).
- Туберкулёз (препарат II ряда).
Парентерально — 15-20 мг/кг/сут в 1-2 введения.
Раствор в ампулах, содержащих 0,1 г, 0,25 г и 0,5 г амикацина; раствор во флаконах, содержащих 1,0 г амикацина.
Адрес этой страницы: http://www.antibiotic.ru/books/mach/mac0108.shtml
Дата последнего изменения: 24.05.2004 18:56
источник
Аминогликозиды – это антибиотики полусинтетического или природного происхождения. Они оказывают бактерицидное действие и уничтожают чувствительные к ним патогенные микроорганизмы.
Аминогликозиды вызывают гибель патогенов лишь в аэробных условиях, они малоэффективны по отношению к анаэробным бактериям. Данная группа насчитывает несколько полусинтетических и около десятка природных антибиотиков, производимых из актиномицетов.
Механизм действия аминогликозидов основан на образовании необратимых ковалентных связей с 30S рибосомальным субъединицам бактерий за счет этого происходит нарушение биосинтеза белков и нарушается воспроизведение генетического материала в бактериях, что приводит к гибели клетки.
На сегодняшний день существует несколько классификаций аминогликозидных антибиотиков: по спектру антимикробной активности, по особенностям развития резистентности при длительном применении препарата, когда в процессе терапии наблюдается редукция или полное прекращение лечебного действия медикамента, по времени введения в клиническую практику.
Одна из самых популярных классификаций предложена И.Б. Михайловым, автором учебника «Клиническая фармакология». В её основу взят спектр действия аминогликозидов и особенности возникновения сопротивляемости и устойчивости бактерий к аминогликозидам. Он выделил 4 генерации (поколения) антибактериальных препарата (далее АБП) данной группы. К антибиотикам аминогликозидам относятся:
- 1 п-ие – стрептомицин ® , канамицин ® , неомицин ® , паромомицин ® ;
- 2 п-ие – гентамицин ® ;
- 3 п-ие – тобрамицин ® , сизомицин ® , амикацин ® ;
- 4 п-ие – изепамицин ® .
По времени введения в клиническую практику и по областям применения предлагают следующую классификацию:
- препараты 1 – ой генерации. Их применяют против микобактерий из группы Mycobacterium tuberculosis complex, являющихся возбудителями туберкулёза. Лекарства первого поколения менее активны по отношению к стафилококкам и грамотрицательной флоре. В современной медицине уже практически не используются, так как устарели.
- препараты 2 – ой генерации. Представителем второй группы является гентамицин ® , отличающийся высокой активностью по отношению к синегнойной палочке. Его внедрение обусловлено возникновением антибиотикорезистентных штаммов бактерий.
- препараты 3 – ей генерации. Аминогликозиды 3 поколения проявляют бактерицидную активность к Enterobacter, Klebsiella, Pseudomonas aeruginosa и Serratia
- препараты 4 – ой генерации. Изепамицин ® показан в лечении нокардиоза, абсцессов головного мозга, менингитов, урологических заболеваний, гнойных инфекций и сепсиса.
Последние поколения были изобретены, когда стали известны молекулярные механизмы резистентности бактерий и обнаружены специфические энзимы, которые инактивируют антимикробный препарат.
Современная фармацевтическая промышленность выпускает множество антибиотических средств, которые представлены в аптеках под следующими торговыми названиями:
Наиболее популярные препараты рассмотрены ниже.
| 1 | Амикабол ® |
| 2 | Амикацин ® |
| 3 | Амикацин-Виал ® |
| 4 | Амикацин-Ферейн ® |
| 5 | Амикацина сульфат ® |
| 6 | Амикин ® |
| 7 | Амикозит ® |
| 8 | Брамитоб ® |
| 9 | Бруламицин ® |
| 10 | Веро-Нетилмицин ® |
| 11 | Гарамицин ® |
| 12 | Гентамицин ® |
| 13 | Гентамицин-АКОС ® |
| 14 | Гентамицин-К ® |
| 15 | Гентамицин-Ферейн ® |
| 16 | Гентамицина сульфат ® |
| 17 | Гентамицина сульфат ® 0,08 г |
| 18 | Гентамицина сульфата ® раствор для инъекций 4% |
| 19 | Гентамициновая мазь ® 0,1% |
| 20 | Дилатерол ® |
| 21 | Изофра ® |
| 22 | Канамицин ® |
| 23 | Канамицина кислого сульфат ® |
| 24 | Канамицина сульфат ® |
| 25 | Канамицина сульфат ® кислый |
| 26 | Кирин ® |
| 27 | Ликацин ® |
| 28 | Небцин ® |
| 29 | Неомицин ® |
| 30 | Неомицина сульфат ® |
| 31 | Нетилмицин Протекх ® |
| 32 | Нетилмицина сульфат ® |
| 33 | Нетромицин ® |
| 34 | Неттависк ® |
| 35 | Неттацин ® |
| 36 | Селемицин ® |
| 37 | Стрептомицин ® |
| 38 | Стрептомицина сульфат ® |
| 39 | Тоби ® |
| 40 | Тоби Подхалер ® |
| 41 | Тобрамицин ® |
| 42 | Тобрамицин-Гобби ® |
| 43 | Тобрацин-АДС ® |
| 44 | Тобрекс ® |
| 45 | Тобрекс 2Х ® |
| 46 | Тобрисс ® |
| 47 | Тобропт ® |
| 48 | Тобросопт ® |
| 49 | Тробицин ® |
| 50 | Фарциклин ® |
| 51 | Хемацин ® |
Наиболее популярные препараты рассмотрены ниже.
Порошок белого цвет, вводимый внутримышечно. Не имеет запаха.
- Показания: первичный туберкулезный комплекс, донованоз, бруцеллёз.
- Применение: индивидуально. Вводят внутримышечно интратрахеально, аэрозольно.
- Побочные эффекты: протеинурия, гематурия, апноэ, невриты, нарушения стула, воспаление зрительного нерва, кожные высыпания. Одновременный приём с капреомицином ® увеличивает риск развития ототоксического действия. В сочетании с миорелаксантами увеличивается риск развития нейро-мышечнойблокады.
- В период терапии стрептомицином необходимо наблюдать за состоянием вестибулярного аппарата и скоростью клубочковой фильтрации.
- Пациентам с патологиями экскреторной системы снижают суточные дозы препарата в зависимости от скорости клубочковой фильтрации.
Аэрозоль или мазь для наружного применения. Однородная консистенция.
- Показания: фурункулы, импетиго, гнойные осложнения при обморожениях и ожогах.
- Особенности применения: перед использованием средства флакон рекомендовано встряхнуть. На пораженные кожные покровы распыляют средство на протяжении трёх секунд. Процедуру повторяют один-три раза за сутки. Препарат применяют около недели.
- Побочные эффекты: аллергия, зуд, крапивница, отёчность. Длительное применение совместно с гентамицином ® , колистином ® приводит к усилению токсического действия.
- Важно избегать попадания в глаза и на слизистые оболочки и в глаза. Не вдыхать распыленный препарат.
Порошок для приготовления раствора.
- Показания: туберкулёз, энтерит, колит, конъюнктивит, воспаления и язвенные поражения роговицы.
- Побочные эффекты: гипербилирубинемия, мальабсорбция, нарушения стула, повышенное газообразование, малокровие, тромбоцитопения, головные боли, потеря чувствительности мышц, эпилепсия, потеря координации, слезотечение, жажда, гиперемия, лихорадка, отёк Квинке.
- Категорически запрещено совместное применение со стрептомицином, гентамицином ® , флоримицином ® . Также не рекомендуется во время терапии канамицином ® принимать мочегонные препараты. В сочетании с β -лактамными антибиотиками у пациентов с тяжёлой почечной недостаточностью происходит инактивация канамицина ® .
Раствор для внутримышечного введения.
- Показания: воспаление желчного пузыря, пиелонефрит, цистит, воспаление лёгких, пиоторакс, перитонит, сепсис. Инфекционные поражения, вызванные ранениями, ожогами, молниеносная язвенная пиодермия, фурункулёз и т.д.
- Побочные эффекты: тошнота, рвота, снижение концентрации гемоглобина, олигоурия, потеря слуха, ангионевротический отёк, кожные высыпания.
- При одновременном применении с индометацином ® снижается скорость выведения препарата. Обезболивающие, вводимые ингаляционно, и гентамицин ® увеличивают риск развития блокады нервно-мышечной передачи.
Раствор для ингаляций и для инъекций.
- Применяется для лечения: сепсиса, воспаления мозговых оболочек, инфекции сердечно-сосудистой и мочеполовой системы, заболеваний дыхательных путей.
- Побочные эффекты: нарушения функций вестибулярного аппарата, тошнота, болевые ощущения в месте укола, понижение содержания кальция, калия и магния в плазме крови.
- Польза антимикробной терапии должна превышать превышает риск развития побочных действий в следующих случаях: у больных с патологиями почек, нарушениями органов слуха, дрожательном параличом. Не рекомендуется совместное применение с диуретиками и миорелаксантами.
Амикацин ® порошок для приготовления раствора.
- Показания: воспаление брюшины, сепсис у новорождённых, инфекции центральной нервной системы и опорно-двигательного аппарата, гнойный плеврит, нарывы.
- Побочные эффекты: повышение температуры тела, сонливость, ухудшение концентрации внимания, вестибулярные нарушения, тревожность, нарушение функции почек, увеличение активности печеночных трансаминаз, тревожность и т.д.
- С осторожностью применяют в лечении пациентов с идиопатическим синдромом паркинсонизма. Режим дозирования корректируют при хронических болезнях почек. Диэтиловый эфир в сочетании с амикацином ® приводит к угнетению дыхательной деятельности.
- Показания: нозокомиальная пневмония, бронхит, острое разлитое гнойное воспаление подкожно-жировой клетчатки, послеоперационные осложнения, сепсис.
- Побочные эффекты: повышение уровня креатинина и небелковых азотистых соединений в сыворотке крови, нарушение функции почек и печени, тревожность, головные боли, эритематозные высыпания, и т.д.
- Сочетание изепамицина с нейромышечных блокаторами чревато возникновения паралича дыхательной мускулатуры. Применение с препаратами пенициллинового ряда нежелательно из-за взаимной потери активности обоих антибиотиков.
Раствор для инъекционного введения.
- Показания: сепсис, инфицированные ожоги, перитонит, абсцесс легких, воспаление уретры, цервицит и т.д.
- Побочные эффекты: болевые ощущения в месте укола, рвота, анемия, лимфоцитопения, головные боли, тревожность, нарушение сна и т.д.
- Противогерпесные и мочегонные усиливают нейротоксический эффект.
Стрептомицин является первым антибиотиком из группы аминогликозидов. Его вывели в 40-х годах прошлого столетия из лучистого гриба стрептомицета. Род Streptomyces является самым крупным родом, синтезирующим АБП, и его используют уже больше 50 лет в промышленном производстве антибактериальных медикаментов.

Новоявленный стрептомицин, механизм действия которого связан с угнетением синтеза белка в клетке патогена, влияет на окислительные процессы в микроорганизме и ослабляет его углеводный обмен. Антибиотики аминогликозиды – препараты, которые стали выпускаться сразу после антибиотиков пенициллинового ряда. Несколько лет спустя фармакология представила миру канамицин.
На заре эры антибиотикотерапии стрептомицин и пенициллин назначались для лечения многих инфекционных заболеваний, которые в современной медицине не считаются показаниями к назначению аминогликозидных лекарств. Бесконтрольное применение спровоцировало появление резистентных штаммов и перекрестной устойчивости. Перекрестная устойчивость – это способность микроорганизмов обладать резистентностью к нескольким антибиотическим веществам со сходным механизмом действия.
Впоследствии стрептомицин стали использовать лишь в составе специфической химиотерапии туберкулеза. Сужение терапевтического диапазона связано с его отрицательным воздействием на вестибулярный аппарат, слух и токсическим действием, проявляющимся поражением почек.
Амикацин ® , относящийся к четвертому поколению, считается препаратом резерва. Он оказывает ярко выраженный эффект, однако отличается толерантностью, поэтому его назначают лишь очень небольшому проценту пациентов.
Аминогликозидные антибиотики назначаются при следующих заболеваниях:
- криптогенном сепсисе;
- инфекционном поражении ткани клапанного аппарата сердца;
- менингитах, возникающих как осложнение при черепно-мозговой травме и экстренном нейрохирургическом вмешательстве;
- нейтропенической лихорадке;
- внутрибольничной пневмонии;
- инфекционном поражении почечной лоханки, чашечек и паренхимы почки (воспаление почек);
- интраабдоминальных инфекциях;
- синдроме диабетической стопы;
- воспалении костного мозга, компактной части кости, надкостницы, а также окружающих мягких тканей;
- инфекционном артрите;
- бруцеллёзе;
- воспалении роговицы;
- туберкулёзе.
Антибактериальные препараты вводят для предупреждения послеоперационных инфекционно-воспалительных осложнений. Аминогликозиды нельзя применять в лечении внебольничной пневмонии. Это обусловлено отсутствием активности антибиотиков в отношении Streptococcus pneumoniae.
Из-за ярко выраженной токсичности не рекомендуется применение аминогликозидных антибиотиков для орошения воспалённых тканей брюшины и проточно-промывного дренирования.
Грамотное назначение аминогликозидов должно сопровождаться:
- строгим расчётом дозировки с учётом возраста, общего состояния здоровья, хронических заболеваний, локализации инфекции и т.д.
- соблюдением режима дозирования, интервалов между приёмами препарата;
- правильным выбором пути введения;
- диагностикой концентрации фармакологического средства в крови;
- мониторингом уровня креатинина в плазме крови. Его концентрация – это важный показатель деятельности почек.
- проведением акуметрии, измеряющей остроту слуха, определяющей слуховую чувствительность к звуковым волнам различной частоты.
Высокий уровень токсичности препаратов может стать причиной:
- снижения чувствительности слухового анализатора, появления посторонних звуков в ушах, ощущением заложенности;
- поражения почек, которое проявляется снижением скорости клубочковой фильтрации жидкости через нефроны (структурно-функциональная единица органа), качественным и количественным изменением мочи.
- головных болей, головокружения, расстройств моторики, или атаксии. Данные побочные эффекты проявляются особенно ярко у людей преклонного возраста.
- вялости, упадка сил, утомляемости, непроизвольных сокращений мышц, снижением чувствительности кожи.
- нейромышечных расстройств, затрудненного дыхания вплоть до полного паралича дыхательных мышц. Побочный эффект усиливается из-за совместного приёма антибиотиков с медикаментозными средствами, которые снижают тонус скелетной мускулатуры. Во время антимикробной терапии аминогликозидами нежелательно проводить переливание цитратной крови, в которую добавляют лимоннокислый натрий, предотвращающий её от свёртывания.
Повышенная чувствительность и склонность к аллергическим реакциям в анамнезе являются противопоказаниям для приёма всех препаратов данной группы. Это связано с возможной перекрёстной гиперчувствительностью.
Системное использование аминогликозидов противопоказано при:
- обезвоживании;
- индивидуальной непереносимости амногликозидов;
- тяжёлой почечной недостаточности;
- поражении преддверно-улиткового нерва;
- миастении;
- болезни Паркинсона.
Лечение аминогликозидами новорождённых, недоношенных детей и пожилых людей не рекомендовано.
Аминогликозиды в таблетках считаются менее эффективными, чем в ампулах. Это связано с тем, что инъекционные формы обладают большей биодоступностью.
Аминогликозиды – это мощные антимикробные препараты, влияние которых на плод до конца не изучено. Известно, что они преодолевают плацентарный барьер, оказывают нефротоксическое действие и в некоторых случаях подвергаются метаболическим превращениям в органах и тканях плода.
Аминогликозиды могут привести к полной двусторонней врождённой глухоте и поражению почек плода.
Поэтому применение аминогликозидов в период вынашивания ребёнка противопоказано.
Препараты аминогликозидного ряда попадают в грудное молоко. Поэтому ппедиатры настоятельно рекомендуют отказаться от лечения антибиотиками во время грудного вскармливания во избежание осложнений.
На нашем сайте Вы можете познакомиться с большинством групп антибиотиков, полными списками входящих в них препаратов, классификациями, историей и прочей важной информацией. Для этого создан раздел «Классификация» в верхнем меню сайта.
источник
Аминогликозиды являются одним из ранних классов антибиотиков. Первый аминогликозид — стрептомицин был получен в 1944 г. В настоящее время выделяют три поколения аминогликозидов.
| I поколение | II поколение | III поколение |
|---|---|---|
| Стрептомицин | Гентамицин | Амикацин |
| Неомицин | Тобрамицин | |
| Канамицин | Нетилмицин |
Основное клиническое значение аминогликозиды имеют при лечении нозокомиальных инфекций, вызванных аэробными грамотрицательными возбудителями, а также инфекционного эндокардита. Стрептомицин и канамицин используют при лечении туберкулеза. Неомицин как наиболее токсичный среди аминогликозидов применяется только внутрь и местно.
Аминогликозиды обладают потенциальной нефротоксичностью, ототоксичностью и могут вызывать нервно-мышечную блокаду. Однако учет факторов риска, однократное введение всей суточной дозы, короткие курсы терапии и ТЛМ могут уменьшить степень проявления НР.
Аминогликозиды оказывают бактерицидное действие, которое связано с нарушением синтеза белка рибосомами. Степень антибактериальной активности аминогликозидов зависит от их максимальной (пиковой) концентрации в сыворотке крови. При совместном использовании с пенициллинами или цефалоспоринами наблюдается синергизм в отношении некоторых грамотрицательных и грамположительных аэробных микроорганизмов.
Для аминогликозидов II и III поколения характерна дозозависимая бактерицидная активность в отношении грамотрицательных микроорганизмов семейства Enterobacteriaceae (E.coli, Proteus spp., Klebsiella spp., Enterobacter spp., Serratia spp. и др.), а также неферментирующих грамотрицательных палочек (P.aeruginosa, Acinetobacter spp.). Аминогликозиды активны в отношении стафилококков, кроме MRSA. Стрептомицин и канамицин действуют на M.tuberculosis, в то время как амикацин более активен в отношении M.avium и других атипичных микобактерий. Стрептомицин и гентамицин действуют на энтерококки. Стрептомицин активен против возбудителей чумы, туляремии, бруцеллеза.
Аминогликозиды неактивны в отношении S.pneumoniae, S.maltophilia, B.cepacia, анаэробов (Bacteroides spp., Clostridium spp. и др.). Более того, резистентность S.pneumoniae, S.maltophilia и B.cepacia к аминогликозидам может быть использована при идентификации этих микроорганизмов.
Несмотря на то, что аминогликозиды in vitro активны в отношении гемофил, шигелл, сальмонелл, легионелл, клиническая эффективность при лечении инфекций, вызванных этими возбудителями, не была установлена.
При приеме внутрь аминогликозиды практически не всасываются, поэтому применяются парентерально (кроме неомицина). После в/м введения всасываются быстро и полностью. Пиковые концентрации развиваются через 30 мин после окончания в/в инфузии и через 0,5-1,5 ч после в/м введения.
Пиковые концентрации аминогликозидов варьируют у различных пациентов, поскольку зависят от объема распределения. Объем распределения, в свою очередь, зависит от массы тела, объема жидкости и жировой ткани, состояния пациента. Например, у пациентов с обширными ожогами, асцитом объем распределения аминогликозидов повышен. Наоборот, при дегидратации или мышечной дистрофии он уменьшается.
Аминогликозиды распределяются во внеклеточной жидкости, включая сыворотку крови, экссудат абсцессов, асцитическую, перикардиальную, плевральную, синовиальную, лимфатическую и перитонеальную жидкости. Способны создавать высокие концентрации в органах с хорошим кровоснабжением: печени, легких, почках (где они накапливаются в корковом веществе). Низкие концентрации отмечаются в мокроте, бронхиальном секрете, желчи, грудном молоке. Аминогликозиды плохо проходят через ГЭБ. При воспалении мозговых оболочек проницаемость несколько увеличивается. У новорожденных в СМЖ достигаются более высокие концентрации, чем у взрослых.
Аминогликозиды не метаболизируются, выводятся почками путем клубочковой фильтрации в неизмененном виде, создавая высокие концентрации в моче. Скорость экскреции зависит от возраста, функции почек и сопутствующей патологии пациента. У больных с лихорадкой она может увеличиваться, при понижении функции почек значительно замедляется. У людей пожилого возраста в результате уменьшения клубочковой фильтрации экскреция также может замедляться. Период полувыведения всех аминогликозидов у взрослых с нормальной функцией почек составляет 2-4 ч, у новорожденных — 5-8 ч, у детей — 2,5-4 ч. При почечной недостаточности период полувыведения может возрастать до 70 ч и более.
Почки: нефротоксический эффект может проявляться повышенной жаждой, значительным увеличением или уменьшением количества мочи, понижением клубочковой фильтрации и повышением уровня креатинина в сыворотке крови. Факторы риска: исходные нарушения функции почек, пожилой возраст, высокие дозы, длительные курсы лечения, одновременное применение других нефротоксичных препаратов (амфотерицин В, полимиксин В, ванкомицин, петлевые диуретики, циклоспорин). Меры контроля: повторные клинические анализы мочи, определение креатинина сыворотки крови и расчет клубочковой фильтрации каждые 3 дня (при уменьшении этого показателя на 50% аминогликозид следует отменить).
Ототоксичность: понижение слуха, шум, звон или ощущение «заложенности» в ушах. Факторы риска: пожилой возраст, исходное нарушение слуха, большие дозы, длительные курсы лечения, одновременное применение других ототоксичных препаратов. Меры профилактики: контроль слуховой функции, включая проведение аудиометрии.
Вестибулотоксичность: нарушение координации движений, головокружение. Факторы риска: пожилой возраст, исходные вестибулярные расстройства, высокие дозы, длительные курсы лечения. Меры профилактики: контроль функции вестибулярного аппарата, включая проведение специальных проб.
Нервно-мышечная блокада: угнетение дыхания вплоть до полного паралича дыхательных мышц. Факторы риска: исходные неврологические заболевания (паркинсонизм, миастения), одновременное применение миорелаксантов, нарушение функции почек. Меры помощи: в/в введение кальция хлорида или антихолинэстеразных препаратов.
Нервная система: головная боль, общая слабость, сонливость, подергивание мышц, парестезии, судороги; при использовании стрептомицина возможно появление ощущения жжения, онемения или парестезий в области лица и полости рта.
Аллергические реакции (сыпь и др.) встречаются редко.
Местные реакции (флебит при в/в введении) отмечаются редко.
Эмпирическая терапия (в большинстве случаев назначают в сочетании с β-лактамами, гликопептидами или антианаэробными препаратами, в зависимости от предполагаемых возбудителей):
Посттравматические и послеоперационные менингиты.
источник
Основными представителями этой группы антибиотиков являются стрептомицин, неомицин, канамицин, гентамицин, амикацин, тобрамицин, сизомицин, мономицин и др. Механизм действия аминогликозидов связывают с непосредственным их влиянием на рибосомы и угнетением синтеза белка. Для аминогликозидов характерен бактерицидный эффект.
Стрептомицин является антибиотиком, продуцируемым Actinomycesglobisporus streptomycini. В медицинской практике применяется стрептомицина сульфат (см. химическую структуру). Активность стрептомицина определяется в единицах действия (ЕД) и в весовых единицах. 1 ЕД стрептомицина основания соответствует 1 мкг.
Стрептомицин имеет широкий спектр противомикробного действия. Наиболее важно его угнетающее влияние на микобактерии туберкулеза, возбудители туляремии, чумы. Кроме того, он губительно действует на патогенные кокки, некоторые штаммы протея, синегнойную палочку, бруцеллы и другие грамотрица тельные и грамположительные бактерии. К стрептомицину нечувствительны анаэробы, спирохеты, риккетсии, вирусы, патогенные грибы, простейшие.
К этому антибиотику относительно быстро развивается привыкание. В ряде случаев наблюдается образование стрсптомицинозависимых штаммов, для роста и размножения которых необходим стрептомицин.
Из желудочно-кишечного тракта препарат всасывается плохо. При внутримышечном введении через 1—2 ч стрептомицин накапливается в плазме крови в максимальных концентрациях. Распределяется он в основном экстрацеллюлярно. Проникает в полости брюшины и плевры, при беременности — в ткани плода. Через гематоэнцефалический барьер, как правило, не проходит; при менингите проницаемость гематоэнцефалического барьера для стрептомицина увеличивается. Снижение концентрации стрептомицина в плазме крови на 50% происходит через 2—4 ч.
Выводится стрептомицин большей частью почками (путем фильтрации) в неизмененном виде. Незначительная часть выделяется с желчью в кишечник.
Применяют стрептомицина сульфат главным образом при лечении туберкулеза1. Кроме того, его используют при лечении туляремии, чумы, бруцеллеза, инфекций мочевыводяших путей, органов дыхания, а также при других заболеваниях. Вводят препарат чаще внутримышечно (1—2 раза в сутки), а также в полости тела. С целью воздействия на кишечную флору стрептомицина сульфат назначают внутрь. Для инъекции под оболочки мозга при менингите используют только стрептомицин-хлоркальциевый комплекс (двойная соль стрептомицина гидрохлорида и кальция хлорида). Последний оказывает меньшее раздражающее действие, чем другие препараты стрептомииина. Однако токсичность стрепто-мицин-хлоркальциевого комплекса значительная, поэтому применяют его лишь в случае крайней необходимости.
Отрицательные эффекты стрептомицина включают неаллергические и аллергические влияния. Наиболее серьезным является ототоксическое его действие. Чаще всего поражается вестибулярная ветвь VIII пары черепных нервов, реже — слуховая ветвь. По мнению ряда авторов, назначение кальция пантотената уменьшает возможность возникновения указанных побочных эффектов. Обладает не-фротоксичностью. Стрептомицин оказывает угнетающее влияние на нервно-мышечные синапсы, что может быть причиной угнетения дыхания. Кроме того, он обладает нефротоксичностью, а также раздражающим эффектом, в связи с чем инъекции его болезненны.
При назначении препаратов стрептомицина отмечаются и аллергические реакции (лихорадка, кожные поражения, эозинофилия, редко анафилактический шок и др.). На фоне действия стрептомицина возможно развитие суперинфекции.
Неомицин представляет собой смесь антибиотиков неомицинов А, В и С, продуцируемых Actinomycesfradiae. Выпускается в виде препарата неомицина сульфата. Обладает широким спектром действия. К нему чувствительны как грамположительные, так и грамотрицательные микроорганизмы. На анаэробы, спирохеты, патогенные грибы и вирусы влияния не оказывает. Устойчивость микроорганизмов к неомицину развивается относительно медленно.
При приеме внутрь препарат всасывается плохо, поэтому его действие при таком пути введения ограничивается в основном пищеварительным трактом. Неомицин используют для лечения энтерита, вызванного чувствительными к нему
микроорганизмами. Рационально его применение при резистентности соответствующих возбудителей к другим антибиотикам. Неомицин может быть полезен при подготовке больных к операции на пищеварительном тракте (с целью частичной «стерилизации» кишечника). Положительным качеством является его высокая активность в отношении кишечной палочки, некоторых штаммов протея и синегнойной палочки. Из побочных эффектов возможны диспепсические нарушения, аллергические реакции, кандидамикоз.
Нередко неомицин применяют местно. Его назначают при лечении инфицированных ран, ряда кожных заболеваний (пиодермии и др.), заболеваний глаз (например, конъюнктивита) и т.д. С неповрежденной кожной поверхности и слизистых оболочек всасывается незначительно. Наружно неомицин в ряде случаев используют совместно с глюкокортикоидами (например, с синафланом или флу метазона пивалатом)1. При этом противомикробный эффект сочетается с противовоспалител ьным.
Парентерально неомицин не используют в связи с его высокой токсичностью в отношении почек (появляется белок в моче) и слухового нерва (возникают шум в ушах и снижение слуха вплоть до полной глухоты). Кроме того, неомицин обладает курареподобной активностью (может вызывать угнетение и остановку дыхания).
Препарат противопоказан при заболеваниях почек и слухового нерва.
Гентамицин продуцируется Micromonospora purpurea и М. echinospora. Выпускается в виде гентамицина сульфата (гарамицин).
Обладает широким спектром действия, включающим грамположительные и грамотрицательные бактерии. Наибольший практический интерес представляет его активность в отношении синегнойной палочки, протея, кишечной палочки, а также стафилококков, устойчивых к бензилпенициллину. Устойчивость к гента-мицину развивается медленно.
Из желудочно-кишечного тракта препарат всасывается недостаточно полно, поэтому для системного действия его назначают внутримышечно. Максимальные количества гентамицина в плазме крови при этом пути введения накапливаются через 60 мин. Противомикробные концентрации сохраняются в организме в течение 8—12 ч. Через гематоэнцефалический барьер в обычных условиях гентамицин почти не проникает. При менингите в ликворе обнаруживаются небольшие его концентрации. Выделяется почками преимущественно в неизмененном виде.
Применяют гентамицин главным образом для лечения заболеваний, вызванных грамотрицательными бактериями. Особенно ценен препарат при инфекции мочевыводящих путей (пиелонефрите, цистите), сепсисе, раневой инфекции, ожогах. Пути введения: внутримышечно или наружно.
Гентамицин менее токсичен, чем неомицин. Однако основные неблагоприятные эффекты, типичные для аминогликозидов, наблюдаются и при использовании гентамицина. Одним из них является ототоксическое действие. В основном гентамицин поражает вестибулярную ветвь VIII пары черепных нервов. Слух страдает реже. Нефротоксичность также выражена в меньшей степени, чем у неоми-цина. Обладает курареподобными свойствами.
Группу аминогликозидов представляет также тобрамицин (бруламицин). Продуцируется Str. tenebrarius. Обладает широким спектром действия. Высокоактивен в отношении синегнойной палочки. Эффективные противомикробные концентрации после однократного введения сохраняются в течение 6—8 ч. Вводят препарат внутримышечно и внутривенно. Выделяется он преимущественно почками. Показания к применению аналогичны таковым для гентамицина и определяются спектром противомикробного действия. Обладает нефро- и ототоксичностью, но менее выраженной, чем у гентамицина.
К аминогликозидам относится также антибиотик сизомицин. Продуцируется Micromonospora inyoensis. Обладает широким спектром противомикробного действия, подобным таковому гентамицина. Активнее последнего в отношении разных видов протея, синегнойной палочки, клебсиелл, энтеробактера.
Устойчивость к сизомицину развивается медленно. Возникает также перекрестная устойчивость ко всем аминогликозидам.
Из пищеварительного тракта препарат всасывается плохо, поэтому его вводят внутримышечно и внутривенно. Около 25% связывается с белками плазмы крови. Периодичность введения в клинических условиях 8 ч.
Показания к применению и побочные эффекты аналогичны таковым для ген-тамицина.
К числу наиболее эффективных аминогликозидов относится амикацин (ами-кин)1. Он является производным канамицина. Из всех аминогликозидов обладает наиболее широким спектром противомикробного действия, включающим аэробные грамотрицательные бактерии (в том числе синегнойную палочку, протей, клебсиеллы, кишечную палочку и др.) и микобактерии туберкулеза. На большинство грамположительных анаэробных бактерий не влияет. Устойчив к действию многих бактериальных ферментов, инактивирующих аминогликозиды. Обладает ототоксичностью и нефротоксичностью. Вводят амикацин внутримышечно и внутривенно.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
источник
Группа аминогликозидов объединяет родственные по химическому строению и антимикробному спектру антибиотики олигосахаридной природы – стрептомицины, гентамицины, неомицины, канамицины, мономицины, тобрамицин и др., а также полусинтетический аминогликозид — амикацин.
Антибиотики аминогликозиды получили свое название в связи с наличием в молекуле аминосахаридов, соединенных гликозидной связью с агликоновым фрагментом. По механизму действия аминогликозиды являются ингибиторами синтеза белка. Аминогликозиды характеризуются широким спектром антимикробного действия.
Первый антибиотик этой группы — стрептомицин — был открыт С.Ваксманом (США) в 1942 г.; применяется в медицинской практике с 1946 г.
В 1955 г. японскими учеными был выделен канамицин. Мономицин выделен в нашей стране Г.Ф.Гаузе в 1962 г. Гентамицин выделен и описан в США в 1962 г.; в нашей стране в медицинской практике применяется с 1976 г.
Аминогликозиды получают методом микробиологического синтеза. Продуцентом стрептомицина является Streptomyces globisporus streptomycini; канамицина — Streptomyces kanamyceticus; гентамицина — Microspora purpurea. Амикацин получают полусинтетическим способом.
Многие аминогликозиды обладают ото- и нефротоксичностью.
По химическому строению антибиотики-аминогликозиды являются гликозидами, состоящими из агликона и сахаров, боль-шинство из которых является аминосахарами.
Агликон аминогликозидов представляет собой циклогексановое кольцо с основными группами при С1 и С3 и гидроксильными группами при С4, С5 и С6
По характеру агликона аминогликозиды делят на 2 группы: стрептидинсодержащие и дезоксистрептаминосодержащие. К 1-й группе относятся стрептомицин, дигидрострептомицин, агликоном у которых является стрептидин; ко 2-й группе — канамицины, гентамицины, неомицины, мономицины, амикацин; агликоном у них является 2-дезоксистрептамин, который отличается от стрептиди-на наличием аминогрупп вместо остатков гуанидина и отсутствием оксигруппы при С2.
Аминогликозиды применяются в медицинской практике в виде солей — сульфатов.
Несколько особняком в этой группе стоит стрептомицин, так как по сути он является антибиотиком-гликозидом т.к. сахарные фрагменты не содержат аминогрупп.
Стрептомицина сульфат-Streptomycini sulfas
Химическое нзвание. Streptomycin sulphate — bis[N,N ‘-bis (aminoiminomethyl) -4-O-[5-deoxy-2-O-[2-deoxy-2-(methylamino)-α-L-glucopyranosyl]-3-C-formyl-α-L-lyxofuranosyl]-D-streptamine] trisulphate.
Агликон стрептомицина- стрептидин представляет собой 1.3-дигуанидино-2,4,5,6-тетраоксициклогексан или спирт инозит, в котором две оксигруппы заменены остатками гуанидина:
Сахарная часть стрептомицина представляет дисахарид стрептобиозамин, построенный из связанных между собой остатков N-метил-L-глюкозамина и L-стрептозы:
Свойства. Порошок белого или почти белого цвета, без запаха. Легко растворим в воде, практически нерастворим в этиловом или метиловом спирте. Гигроскопичен. Оптическое вращение от –78 до -83° (35 водный раствор).
Получение. Промышленными продуцентами стрептомицина служат штаммы актиномицетов Actinomyces streptomycini, Streptomyces griseus и др. Процессы ферментации осуществляют из наиболее активных штаммов, оптимизированных сред и других условий, обеспечивающих максимальный выход антибиотика. Затем из культуральной жидкости сорбируют стрептомицин, многократно пропуская через катиониты и затем очищают оксидом алюминия.
Химические свойства. Стрептомицин проявляет основные свойства ввиду наличия в молекуле азотсодержащих (двух гуаниди-новых и одной N-метильной) групп. Поэтому он легко образует со-ли (сульфат, гидрохлорид) и комплексы с ионами некоторых двухзарядных металлов. Применяют в медицине стрептоми-цина сульфат.
В слабокислой среде растворы стрептомицина устойчивы. Подобно другим гликозидам, он легко гидролизуется под действием сильных кислот с образованием стрептидина и стреп-тобиозамина. Стрептобиозамин затем распадается на N-метил-L-глюкозамин и L-стрептозу. Еще быстрее инактивируется стрепто-мицин в щелочной среде (на 50% в течение 3 ч под действием 0,1 М раствора гидроксида натрия). Однако при этом потеря активности обусловлена дегидратацией и изомеризацией L-стрептозы, которая превращается в мальтол (α-метил-β-окси-γ-пирон):
Подлинность. 1.ТСХ на силикагеле, содержащем поли-мер карбомер в сравнении с ГСО стрептомицина. Для сравне-ния используют растворы ГСО канамицина, ГСО неомицина.
2.Взаимодействие с хлоридом железа после щелочного гидролиза. В этом случае мальтол образуется значительно быстрее (в течение 4 мин), если стрептомицин нагревать с 0,5 М раствором гидроксида натрия на кипящей водяной бане. При взаимодействии с ионами железа (II!) в кислой среде мальтол превращается в соединение, имеющее фиолетовую окраску. Эту цветную реакцию используют для испытания подлинности стрептомицина. Она может быть применена и для его фотометрического определения. Мальтольная проба обусловлена наличием альдегидной группы в молекуле стрептомицина. Тест используется в Британской фармакопее (В).
3.Гуанидиновый фрагмент идентифицируется по реакции с альфа-нафтолом в присутствии гипобромида (или гипохлорита) натрия. В этом случае происходит окислительное бромирование (или хлорирование) и образуется соединение хиноидного типа, окрашенное в красно-фиолетовый цвет:
4. При кислотном гидролизе стрептомицина образуются агликон стрептидин и сахарная часть в виде биозы – стрептобиозамина:
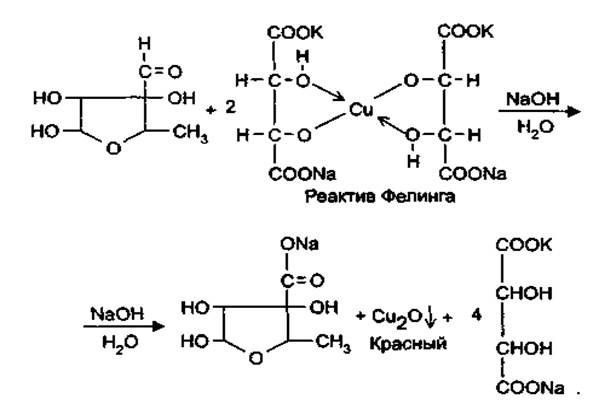
Альдегидная группа проявляет восстановительные свойства, обуславливая тем самым взаимодействие с реактивом Несслера с образованием металлической ртути (бурый осадок) и реактивом Фелинга, с образованием красного осадка оксида меди (1).
5.При конденсации альдегидной группы с фенолами, после нагревания стрептомицина с минеральной кислотой с резорцином образуется вишнево-красное окрашивание, с альфа-нафтолом (Британская фармакопея) – желтое окрашивание.
6.Гуанидиновый фрагмент может быть обнаружен также при щелочном гидролизе. Стрептидин представляет собой двухосновное соединение; при действии щелочью он превращается сначала в производное мочевины, а затем — в стрептамин:
При нагревании со щелочью выделяется аммиак.
8.По реакции образования пикрата стрептидина с т.пл. 283-284°C.
9.Для установления подлинности стандартного образца стрептомицина, используемого для биологического теста и ТСХ используют ЯМР спектроскопию.
Примеси НД не нормируются.
Количественное определение. 1.Фотоколориметрический метод с хлорным железом по мальтолу. Сравнивают оптическую плотность стандартного образца и высушенной субстанции.
2.Биологический метод определение активности методом диффузии в агар. Он должен быть не менее 730 МЕ/мг в пересчете на сухое вещество. 1 мкг химически чистого стрептомицина дол-жен соответствовать 1МЕ.
3.Трилонометрическим методом определяют количество сульфатов по связанному объему бария хлорида. Индикатор металлофталеин.
Применение. Антибиотик широкого спектра действия. Применяют, главным образом для лечения туберкулеза, редко бруцеллеза, чумы, сапа, мелиоидоза и др. Ототоксичен и нефротоксичен.
Форма выпуска. Стерильная рассыпка во флаконах по 250000, 500000, 1000000 МЕ для приготовления раствора для парентерального введения.
Хранение. В сухом помещении при температуре не выше 25°C.
Дигидрострептомицин, который вместо альдегидной группы в остатке L-стрептозы содержит оксиметильную группу, не образует мальтола, что отличает его от стрептомицина.
Антибиотики-аминогликозиды.
Канамицина сульфат — kanamycini monosulfas
Группа антибиотиков – канамицинов, продуцируемых лучистым грибом – Streptomyces kanamiceticus, включает три близких по структуре препарата: Канамицин А, канамицин В, канамицин С. Наименьшую токсичность проявляет канамицин А, его содержание составляет 94%. В его структуру входит агликон мезо-1.3-диамино-4.5.6 триоксициклогексан и два остатка сахаров: 6-амино-6-дезокси-D-глюкоза и 3-амино-3-дезокси- D-глюкоза.
Название. Kanamycin monosulphate это 6-O-(3-amino-3-deoxy-α-D-glucopyranosyl) -4-O-(6-amino-6-deoxy-α-D-glucopyranosyl)-2-deoxy-D-streptamine sulphate.
Свойства. Белый кристаллический порошок без запаха и вкуса. Устойчив к воздействию воздуха. Легко растворим в воде. Показатель оптического вращения плоскости поляризованного света от +112 до +123 (1% раствор в воде, не содержащей СО2).
Получение. Биосинтез. Химочистка включает выделение антибиотика из культуральной жидкости с помощью ионообмен-ных смол, десорбцию, очистку углем и переосаждение метанолом из водного раствора.
Подлинность. 1.ТСХ в сравнении со стандартным образцом канамицина А.
3. Канамицина моносульфат как гликозид способен гидролизо-ваться в кислой среде; при кипячении с кислотами он подвергается гидролитическому расщеплению с полной потерей активности. В отличие от стрептомицина, канамицин устойчив в растворах щелочей. После кислотного гидролиза канамицин дает реакции на сахара (с реактивами Фелинга, Несслера, аммиачным раствором серебра нитрата).
4. При взаимодействии сахарных компонентов канамицина (например, 6-глюкозамина) с концентрированной соляной кислотой образуется 5-аминофурфурол, который можно обнаружить с орцином в присутствии железа (III) хлорида. Предполагают, что реакция протекает следующим образом:
5.Испытания на токсичность. Данное испытание обусловлено высокой токсичностью примеси – канамицина В.
Примеси. Регламентируемыми примесями являются изомеры канамицина: канамицин В (не выше 5%) и канамицин С. Определяют ТСХ в сравнении со стандартными образцами. Количественно определяют примеси по интенсивности пятна в сравнении со стандартом.
Количественное определение. 1.Микробиологический метод диффузии в агар.
2.Поляриметрический метод. Метод находит применение в процессе получения антибиотика, в том числе и в культуральной жидкости.
3.Фотоколориметрический по образованию окрашенного продукта с орцином или нафтолом.
Применение. Антибиотик широкого спектра действия. Применяется главным образом для лечения туберкулеза. Ототоксичен, действует на глазной нерв.
Форма выпуска. В форме моносульфата канамицин выпускается в виде таблеток 0,25 г. канамицин дисульфат порошок 0,5 и 1,0 г для приготовления раствора для парентерального введения или внутривенного капельного введения.
Хранение. Список Б.
Амикацина сульфат — Amicacini sulfas
Свойства. Аморфный порошок белого или белого с желто-ватым оттенком цвета. Легко растворим в воде. Гигроскопичен. Удельное вращение от + 76 до +84° (5% водный раствор).
Получение. Полусинтетический аминогликозидный анти-биотик. Получают из канамицина А. Первоначально защищают аминогруппу в положении 6 аминогликозидного фрагмента и затем вводят ацильный остаток в аминогруппу агликонового фрагмента. Восстановлением снимают защиту и получают амикацин.
Подлинность. 1.ИК спектроскопия в сравнении со стандартным образцом.
2.ТСХ в сравнении со стандартными образцами амикацина и канамицина.
Химические методы. 4.Амикацин, как гликозид подвергает-ся гидролитическому расщеплению с полной потерей активности. После кислотного гидролиза амикацин дает реакции на сахара ( с реактивами Фелинга, Несслера, аммиачным раствором серебра и др.).
5.При нагревании с концентрированными минеральными кислотами амикацин образует 5-аминометилфурфурол, который определяют по цветной реакции с антроном:
6.В отличие от канамицина, амикацин за счет амидной груп-пы образует окрашенные комплексы с солями тяжелый металлов. Для идентификации амикацина применяется реакция с кобальта нитратом после нейтрализации раствором натрия гидроксида (фио-летовое окрашивание).
Примеси. Нормируются 4 различных производных по аминогруппам агликона. Все они хорошо проявляются на ВЭЖХ при наличии стандартных образцов. Типичная хроматограмма приведена на рисунке (из ВР):
Общая формула для примесей приведена ниже. Все они являются побочными продуктами синтеза амикацина:
A. R1 = R3 = Н, R2 = acyl: 4-O-(3-amino-3-deoxy-α-D-glucopyra-nosyl)-6-O-(6-amino-6-deoxy-α-D-glucopyranosyl)-1-N-[(2S)-4-amino-2-hydroxybutanoyl]-2-deoxy-L-streptamine,
B. R1 = R2 = acyl, R3 = H: 4-O-(3-amino-3-deoxy-α-D-glucopyra-nosyl)-6-0-(6-amino-6-deoxy-α-D-glucopyranosyl)-1,3-N-bis[(2S)-4-amino-2-hydroxybutanoyl]-2-deoxy-L-streptamine,
C. R1 = R2 = H, R3 = acyl: 4-0-(6-amino-6-deoxy-α-D-glucopyra-nosyl)-6-O-[3-[[(2S)-4-amino-2-hydroxybutanoyl]amino]-3-deoxy-α-D-glucopyranosyl]-2-deoxy-D-streptamine,
D. R1 = R2 = R3 = H: kanamycin.
Количественное определение. 1. ВЭЖХ. 2.Биологитческий тест методом диффузии в агар.
Применение. Антибиотик широкого спектра действия. Тяжелые инфекции, вызванные как грамположительными , так и грамотрицательными микроорганизмами: остеомиелдит, менингит, сепсис, реже некоторые формы туберкулеза, активен в отношении псевдомонад.
Форма выпуска. Раствор для инъекций 100 мг в 2 мл и 500 мг в 2 мл.
Хранение. Список Б.
Генатмицина сульфат — Gentamycini sulfas
Комплекс антибиотиков, продуцируемых Micromonospora purpurea n. sp., — Гентамицин С1, Гентамицин С2, Гентамицин С1А, Гентамици С2а и Гентамицин С2b (в виде сульфата):
Свойства. Белый порошок или пористая масса с кремоватым оттенком. Легко растворим в воде. Гигроскопичен. Удельное вращение от + 107 до + 121°.
Получение. Получают микробиологическим путем. Очистка через ионообменные смолы.
Подлинность. 1.ТСХ в сравнении со стандартным образцом. 2.ВЭЖХ
Примеси. ВЭЖХ нормируются в качестве примесей сизомицин, гарамин, гентамицин В1 и еще два продукта деструкции препарата.
Количественное определение. 1. ВЭЖХ.
2.Микробиологический метод диффузии в агар.
Применение. Антибиотик широкого спектра действия. Ототоксичен, нефротоксичен.
Форма выпуска. Раствор для инъекций 20 мг/ 2 мл; 40 мг/2 мл; 80 мг/2 мл; 120 мг/мл. Раствор для инъекций 0,3%; мазь для 0,1%.
Хранение. Список Б.
Свойства. Белый или почти белый кристаллический поро-шок. Легко растворим в воде, очень мало в спирте. РН от 9,0 до 11,0. Оптическое вращение от +138 до +148° 4% раствор в воде.
Получение. Биосинтез. Продуцент Streptomyces tenebrarius. Химочистка – ионообменные смолы.
Подлинность. 1. ЯМР в тяжелой воде. 2.ТСХ. 3.С нингидрином на водяной бане дает фиолетово-голубюое окрашивание.
Примеси. ВЭЖХ. Нормируются 3 примеси, в т.ч. канамицин В.
Количественное определение. 1. ВЭЖХ.
Применение. Высокоэффективный антибиотик резерва.
Форма выпуска. Раствор для инъекций 20мг/2 мл; 40 мг/2 мл; 80 мг/2 мл.
Хранение. Список Б.
Ансамицины. Ансамицины – группа антибиотиков, образу-емых лучистым грибком Streptomyces mediterranei. Получают обычно с частичным изменением структуры синтезом как рифам-пицин, так и полусинтетический антибиотик рифабутин.
Рифампицин-Rifampicin
Название. Rifampicin is (2S,12Z,14E,16S,17S,18R,19R,20R, 21S,22R,23S,24Е)-5,6,9,17, 19-pentahydroxy-23-methoxy-2,4,12,16, 18,20,22-heptamethyl-8-[[(4-methylpiperazin-1 -yl) imino]methyl]-1,11 -dioxo-1,2-dihydro-2,7-(epoxypentadeca[1,11,13]trienimino)naphtho[2,1 —b] furan-21-yl acetate.
Свойства. Красно-коричневый или коричнево-красный крис-таллический порошок, мало растворим в воде, растворим в метаноле, мало растворим в ацетоне и спирте этиловом.
Получение. Полусинтетический антибиотик. Получают из природного кето-производного взаимодействием с 1-амино-4-метилпиперазином.
Подлинность. 1. ИК спектр. См. рисунок.
2.УФ спектрофотометрия. Раствор в метаноле дает 4 максиму-ма при 237 нм, 254 нм, 334 нм и 475 нм.
4.При перемешивании раствора рифампицина с персульфатом аамония происходит изменение окраски с оранжево-красной до красно-фиолетовой.
Примеси. Нормируется две основные примеси: рифампицина хинон (примесь А) и рифампицина N-оксид. Метод определения ВЭЖХ.
Количественное определение. 1.УФ спектрофотолметрия.
Применение. Антибиотик широкого спектра действия. Преимущественно используют для лечения туберкулеза. Активен в отношении грамотрицательных микроорганизмов, малочувстви-тельных к другим антибиотикам.
Форма выпуска. Капсулы по 150 и 300 мг. Оральная суспензия.
Хранение. Список Б.
Свойства. Красно-фиолетовый аморфный порошок. Мало растворим в воде, растворим в метаноле, мало растворим в этаноле.
Получение. Полусинтетический антибиотик.
Подлинность. 1. ИК спектр.
Химические методы не описаны.
Примеси. Контролируются ВЭЖХ 4 примеси.
Количественное определение. 1. УФ спектрофотометрия.
Применение. Антибиотик широкого спектра действия. В основном используется в лечении туберкулеза.
Форма выпуска. Капсулы по 150 мг.
Хранение. Список Б.
Гликопептидные антибиотики. Эта группа немногочислен-ных антибиотиков нового поколения – высокомолекулярные углеводсодержащие вещества.
Свойства. Белый или почти белый кристаллический поро-шок. Гигроскопичен. Легко расвторим в воде, мало – в этаноле.
Получение. Биосинтез. Продуцент Amycolatopsis orietalis.
Подлинность. 1.УФ спектрофотометрия. 2.ВЭЖХ.
Примеси. Нормируются 3 примеси. Метод ВЭЖХ.
Количественное определение. 1. Метод диффузии в агар.
Применение. Лечение тяжелых инфекций различной этиологии.
Форма выпуска. Порошок для инъекций 0.5 г и 1,0 г.
Антибиотики макролиды и азалиды.
Основу антибиотиков макролидов составляет макроциклическое лактонное кольцо с 12-17 атомами углерода в цикле. Из этой группы антибиотиков в медицинской практике применяют эритромицин, азитромицин, олеандомицин, кларитромицин, рокситромицин, спирамицин и некоторые другие.
Особенностью строения эритромицина и азитромицина является наличие в цикле агликона Эритронолида, к которому присоединены аминосахар и нейтральнгый сахар.
Эритромицин-Erythromycin
Название. Смесь макролидных антибиотиков, преимущес-твенно содержится эритромицин А — (3R,4S,5S,6R,7R,QR, 11R, 12R, 13S, 14R)-4-[(2,6-dideoxy-3-C-methyl-3-O-methyl-α-l-ribo-hexopy-ranosyl)oxy]-14-ethyl-7,12,13-trihydroxy-3,5, 7,9,11,13-hexamethyl-6-[(3,4,6-trideoxy-3-dimethylamino-β-d-xylo-hexopyranosyl)-oxy] oxacyclotetradecane-2,10-dione (erythromycin A).
Химический состав эритромицинов.
| Агликон | Аминосахар | Нейтральный сахар | |
| Эритромицин А | Эритронолид А | Дезозамин | Кладиноза |
| Эритромицин В | Эритронолид В | Дезозамин | Кладиноза |
| Эритромицин С | Эритронолид С | Дезозамин | Микароза |
Эритронолид по химическому строению представляет собой циклическую систему, состоящую из 13 углеродных атомов и включающие лактонные кольца:
Аминосахара в эритромицинах одинаковые – дезозамин:
Нейтральные сахара – кладиноза и микароза:
Свойства. Кристаллы или порошок белого или белого с желтоватым оттенком цвета. Гигроскопичен. Содержание эритромицина В не более 5% и эритромицина С – не более 5%. Удельное вращение от –71 до -78° (2% раствор в этаноле ВР). Мало растворим в воде, растворимость уменьшается с увеличением температуры. Легко растворим в этаноле, растворим в метаноле.
Получение. Биосинтез. Продуцент Streptomyces erythreus. Химочистка включает экстракцию из культуральной жидкости с последующей очисткой.
Подлинность. 1. ИК спектр (см. рисунок) в сравнении со стандартным образцом эритромицина..
Химические реакции. 4.При нагревании на водяной бане с ксангидролом появляется красное окрашивание.
5.При растворении в ацетоне и концентрированной соляной кислоте раствор приобретает оранжевое окрашивание, переходящее в красное.
Примеси. Нормируется содержание основных примесей – эритромицина В и эритромицина С ( не более 5% каждой). Кроме того определяют ВЭЖХ минорные притмеси: эритромицин F, эритромицин Е, ангидроэритромицин А, и др. всего 6 примесей.
Количественное определение. 1. Диффузией в агар на культуре Bacillus cereus.
Применение. Антибиотик широкого спектра действия.
Форма выпуска. Капсулы и таблетки, в т.ч. покрытые кишенчнорастворимой оболочкой по 0,25 г. Эритромицин фосфат используется для внутривенного введения.
Хранение. Список б в защищенном от света месте.
Азитромицин — Azithromycin
Аглюкон азитромицина отличается наличием N-метильной группы в положении 10 лактонного макроцикла.
Свойства. Белый или почти белый кристаллический поро-шок. Практически нерастворим в воде, легко растворим в этаноле и метиленхлориде. Оптическое вращение от –45 до -49° (1% раствор в этаноле).
Получение. Полусинтетический антибиотик. Синтез описан в патентной литературе.
Подлинность. 1. ИК спектр в сравнении со стандартным образцом.
Примеси. Нормируется более 10 различных примесей.
Количественное определение. 1. ВЭЖХ.
2.Биологический метод диффузии в агар.
Применение. Высокоэффективный антибиотик широкого спектра действия. Эффективен при урогенитальных инфекциях.
Форма выпуска. Таблетки и капсулы 125 мг, 500 мг, 250 мг. Порошок для приготовления оральных суспензий по 100 мг и 200 мг.
Хранение. Список Б.
Олеандомицин-
Свойства. Белый или желтоватый кристаллический порошок.
Получение. Биосинтез. Продуцент Streptomyces antibioticus.
Подлинность. ИК спектр и хроматография.
Количественное определение. Метод диффузии в агар.
Форма выпуска. Таблетки, в т.ч. композитные – олететрин.
источник